题目内容
5.已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3kJ/mol,下列说法中正确的是( )| A. | 浓硫酸和NaOH溶液反应,生成 l mol水时放热57.3 kJ | |
| B. | 含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ | |
| C. | 1L 0.l mol/L CH3COOH与1L 0.l mol/L NaOH溶液反应后放热为5.73 kJ | |
| D. | 1L 0.l mol/L HNO3与 1L 0.l mol/L NaOH溶液反应后放热为 5.73 kJ |
分析 A、浓硫酸稀释放出大量的热;
B、NaOH足量,1mol H2SO4的稀硫酸与2molNaOH溶液中和生成2mol水;
C、醋酸是弱电解质,电离需吸收热量;
D、硝酸为强酸,氢氧化钠为强碱,二者的稀溶液反应生成0.1molH2O后放热为5.73 kJ.
解答 解:A、浓硫酸稀释放出大量的热,浓硫酸与稀NaOH溶液完全反应生成1mol水时放出的热量包括中和热和溶解热,故大于57.3 kJ,故A错误;
B、NaOH足量,1mol H2SO4的稀硫酸与2molNaOH溶液中和后,放热为114.6kJ,故B错误;
C、醋酸是弱电解质,电离需吸收热量,稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量小于57.3 kJ,故C错误;
D、硝酸为强酸,氢氧化钠为强碱,1L0.1 mol/L HNO3与1L 0.1mol/L NaOH溶液反应后放热为5.73 kJ,故D正确;
故选D.
点评 本题考查学生对于反应热、中和热的理解及有关计算等,难度不大,注意强酸、强碱的稀溶液中和热为57.3kJ/mol.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列说法正确是( )
| A. | 含有极性键的分子一定是极性分子 | B. | 单质分子一定是非极性分子 | ||
| C. | 氢键一定与氢元素有关 | D. | 共价键只存在于非金属元素之间 |
16.常温下,1.0mol/L一元酸HA与等体积等浓度KOH溶液混合,所得溶液粒子的浓度关系如表(不含水分子的5种粒子,A为短周期元素),下列说法正确的是( )
| 粒子 | K+ | A - | X | Y | Z |
| 浓度(mol/L) | 0.50 | 0.49 | c(X)>c(Y)>c(Z) | ||
| A. | 元素A最高价氧化物对应水化物为HAO4 | |
| B. | 表格中X表示HA,Y表示H+ | |
| C. | 所得溶液中c(X)+c(A-)=c(K+) | |
| D. | 等体积等浓度的HA和盐酸分别加水稀释10倍后,pH (HA)>pH(HCl) |
20.下列有关热化学方程式的叙述正确的是( )
| A. | 已知2H2 (g)+O2(g)═2H2O(g )△H=-483.6kJ/mol,则H2的燃烧热为△H=-241.8kJ/mol | |
| B. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4kJ/mol | |
| C. | 反应NH3(g)+HCl(g)═NH4Cl (s)△H<0,该反应在任何温度下都可自发进行 | |
| D. | 已知C(s)+O2(g)═CO2(g)△H1;C(s)+$\frac{1}{2}$O2(g)═CO(g)△H2,则△H1>△H2 |
17.下列关于硅酸的说法正确的是( )
| A. | 硅酸可以通过SiO2和水化合反应直接制得 | |
| B. | 可用反应Na2SiO3+2HCl═2NaCl+H2SiO3↓制取硅酸 | |
| C. | 因为硅酸难溶于水,所以它不能与NaOH溶液反应 | |
| D. | 干燥剂“硅胶”的主要成分是硅酸钠 |
15.用酸性氢氧燃料电池为电源进行电解的实验装置如图所示.下列说法中正确的是( )
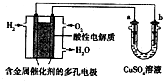

| A. | 燃料电池工作时,正极反应为:O2+4H++4e-═2H2O | |
| B. | a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 | |
| C. | a极是纯铜,b极是粗铜时,可以达到铜的精炼目的 | |
| D. | a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
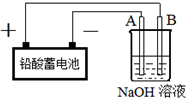 Cu2O是一种半导体材料,实验室用铅酸蓄电池电解一定浓度的NaOH溶液制备Cu2O,方程式为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑装置如图所示,回答下列问题
Cu2O是一种半导体材料,实验室用铅酸蓄电池电解一定浓度的NaOH溶液制备Cu2O,方程式为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑装置如图所示,回答下列问题