题目内容
9.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如表.表1 几种砷酸盐的Ksp
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 浓度 | 28.42g•L-1 | 1.6g/L |
| 排放标准 | pH=6~9 | 0.5mg/L |
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=0.29mol/L.
(2)向Al3+、Fe3+的混合溶液中加入Na3AsO4溶液,当两种沉淀共存时,溶液中c(Al3+)和c(Fe3+)的比值为2.8×104.
(3)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降.
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为CaSO4.
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为H3AsO4是弱酸,当溶液中pH调节到8左右时,酸碱反应,使溶液中AsO43-浓度增大,至Qc>Ksp,Ca3(AsO4)2开始沉淀.
分析 (1)由表格数据可知,硫酸浓度为28.42g•L-1,结合n=$\frac{m}{M}$计算;
(2)向Al3+、Fe3+的混合溶液中加入Na3AsO4溶液,当两种沉淀共存时,溶液中c(Al3+)和c(Fe3+)的比值为$\frac{Ksp(AlAs{O}_{4})}{Ksp(FeAs{O}_{4})}$;
(3)①先向废水中投入生石灰调节pH到2,钙离子与硫酸根离子结合生成沉淀;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀,Qc>Ksp,以此来解答.
解答 解:(1)由表格数据可知,硫酸浓度为28.42g•L-1,则硫酸的物质的量浓度c(H2SO4)=$\frac{28.42g/L}{98g/mol}$=0.29mol/L,
故答案为:0.29;
(2)向Al3+、Fe3+的混合溶液中加入Na3AsO4溶液,当两种沉淀共存时,溶液中c(Al3+)和c(Fe3+)的比值为$\frac{Ksp(AlAs{O}_{4})}{Ksp(FeAs{O}_{4})}$=$\frac{1.6×1{0}^{-16}}{5.7×1{0}^{-21}}$=2.8×104,
故答案为:2.8×104;
(3)①先向废水中投入生石灰调节pH到2,钙离子与硫酸根离子结合生成沉淀,则沉淀主要成分的化学式为CaSO4,故答案为:CaSO4;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为H3AsO4是弱酸,当溶液中pH调节到8左右时,酸碱反应,使溶液中AsO43-浓度增大,至Qc>Ksp,Ca3(AsO4)2开始沉淀,故答案为:H3AsO4是弱酸,当溶液中pH调节到8左右时,酸碱反应,使溶液中AsO43-浓度增大,至Qc>Ksp,Ca3(AsO4)2开始沉淀.
点评 本题考查混合物分离提纯综合应用,为高频考点,把握习题中表格数据、沉淀生成及转化及混合物分离方法为解答的关键,侧重分析与应用、实验能力的综合考查,题目难度不大.

| A. | 硫酸亚铁酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O | |
| B. | 过量石灰水与碳酸氢钙反应:Ca2++2HCO${\;}_{3}^{-}$+2OH-═CaCO3↓+CO${\;}_{3}^{2-}$+2H2O | |
| C. | 向偏铝酸钠溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO${\;}_{3}^{-}$ | |
| D. | 过量铁和稀硝酸反应:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
| A. | 标准状况下,22.4 L H2O中含有的分子数为NA | |
| B. | 32g O2中含有的分子数为NA | |
| C. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数一定为0.2NA | |
| D. | 1 L 1 mol•L-1 CaCl2溶液中含有的氯离子数为NA |

| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 工业上金属钠是通过氯碱工业进行制取 | |
| C. | 第③步中结晶出的MgCl2•6H2O可在空气中受热分解制无水MgCl2 | |
| D. | 第④步中溴元素被氧化,第⑤步中既有溴元素被氧化也有溴元素被还原 |

| A. | 该反应的热化学方程式为$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g)△H=-92kJ•mol-1 | |
| B. | 不用催化剂,生成1molNH3放出的热量为46kJ,加入催化剂,生成1molNH3放出的热量为小于46kJ | |
| C. | 加入催化剂,降低了正反应的活化能,升高了逆反应的活化能 | |
| D. | 在温度、体积一定的条件下,通入1molN2和3molH2,反应后放出的热量为Q1,若通入2molN2和6molH2,反应后放出的热量为Q2,则Q1<0.5Q2<92KJ |
 .
.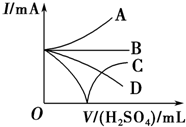 向Ba(OH)2溶液中加入稀硫酸,请完成下列问题:
向Ba(OH)2溶液中加入稀硫酸,请完成下列问题: