题目内容
五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构.A和B、D、E均能形成共价型化合物.A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性.回答下列问题:
(1)五种元素中,原子半径最大的是 ,非金属性最强的是 (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是 (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为 ,其中存在的化学键类型为 ;
(4)D最高价氧化物的水化物的化学式为 ;
(5)单质E与水反应的离子方程式为 .
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为
(4)D最高价氧化物的水化物的化学式为
(5)单质E与水反应的离子方程式为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:五种短周期元素A、B、C、D、E的原子序数依次增大.A和B形成的共价化合物在水中呈碱性,该化合物为NH3,则A为氢元素、B为氮元素;A和C同族,C的原子序数大于氮元素,故C为Na元素;B和D 同族,则D为磷元素;C和E形成的化合物在水中呈中性,则E为Cl元素,验证符合,据此解答.
解答:
解:五种短周期元素A、B、C、D、E的原子序数依次增大.A和B形成的共价化合物在水中呈碱性,该化合物为NH3,则A为氢元素、B为氮元素;A和C同族,C的原子序数大于氮元素,故C为Na元素;B和D 同族,则D为磷元素;C和E形成的化合物在水中呈中性,则E为Cl元素,
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故Na元素的原子半径最大;
最高价含氧酸的酸性越强,中心元素的非金属性越强,高氯酸是最强的含氧酸,故Cl非金属性最强;
故答案为:Na;Cl;
(2)由A和B、D、E所形成的共价型化合物分别为NH3、PH3、HCl,非金属性越强氢化物越稳定,故热稳定性最差的是 PH3,
故答案为:PH3;
(3)A和E形成的化合物HCl,A和B形成的化合物NH3,二者反应生成NH4Cl,NH4Cl晶体中含有:离子键、共价键,
故答案为:NH4Cl;离子键、共价键;
(4)P元素的最高价氧化物的水化物的化学式为H3PO4,故答案为:H3PO4;
(5)氯气与水反应生成盐酸与次氯酸,反应离子方程式为:Cl2+H2O=H++Cl-+HClO,故答案为:Cl2+H2O=H++Cl-+HClO.
(1)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故Na元素的原子半径最大;
最高价含氧酸的酸性越强,中心元素的非金属性越强,高氯酸是最强的含氧酸,故Cl非金属性最强;
故答案为:Na;Cl;
(2)由A和B、D、E所形成的共价型化合物分别为NH3、PH3、HCl,非金属性越强氢化物越稳定,故热稳定性最差的是 PH3,
故答案为:PH3;
(3)A和E形成的化合物HCl,A和B形成的化合物NH3,二者反应生成NH4Cl,NH4Cl晶体中含有:离子键、共价键,
故答案为:NH4Cl;离子键、共价键;
(4)P元素的最高价氧化物的水化物的化学式为H3PO4,故答案为:H3PO4;
(5)氯气与水反应生成盐酸与次氯酸,反应离子方程式为:Cl2+H2O=H++Cl-+HClO,故答案为:Cl2+H2O=H++Cl-+HClO.
点评:本题考查位置结构性质关系、常用化学用语、元素周期律、化学键等,难度中等,推断元素是解题的关键,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列各组离子反应可用H++OH-=H2O表示的是( )
| A、氢氧化钡和硫酸 |
| B、氢氧化铜和盐酸 |
| C、盐酸和氢氧化钠 |
| D、硫酸和氢氧化镁 |
分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A、H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
| B、HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 |
| C、HF、CH3CH2OH、KOH都易溶于水,都是电解质 |
| D、HCOOH、H2CO3、H2S分子中均含有两个氢原子,都是二元酸 |
下列说法正确的是( )
| A、相对分子质量相同的物质是同种物质 |
| B、赤潮发生的根本原因是含氟制冷剂大量使用导致臭氧层破坏的结果 |
| C、具有同一通式的物质属于同系物 |
| D、含氮、磷的大量污水直接排入大海,是赤潮发生的直接原因 |
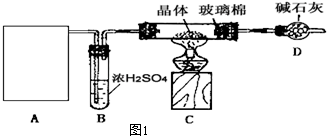

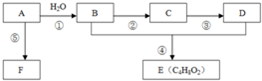 通过石油裂解可以获得A,再以A为原料还可以合成很多的化工产品.已知F可作为保鲜膜的材料,E是有香味的液体.试根据如图回答有关问题:
通过石油裂解可以获得A,再以A为原料还可以合成很多的化工产品.已知F可作为保鲜膜的材料,E是有香味的液体.试根据如图回答有关问题: