题目内容
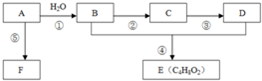 通过石油裂解可以获得A,再以A为原料还可以合成很多的化工产品.已知F可作为保鲜膜的材料,E是有香味的液体.试根据如图回答有关问题:
通过石油裂解可以获得A,再以A为原料还可以合成很多的化工产品.已知F可作为保鲜膜的材料,E是有香味的液体.试根据如图回答有关问题:(1)有机物A的名称为
(2)写出图示反应②、⑤的化学方程式,并指明反应类型:
②
考点:有机物的推断
专题:有机物的化学性质及推断
分析:B转化得到C,C进一步转化得到D,则C与D反应生成E,E是有香味的液体,结合E的分子式可知,E为CH3COOCH2CH3,则B为CH3CH2OH,C为CH3CHO,D为CH3COOH,故A为CH2=CH2,乙烯发生加聚反应的F为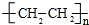 ,据此解答.
,据此解答.
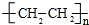 ,据此解答.
,据此解答.解答:
解:B转化得到C,C进一步转化得到D,则C与D反应生成E,E是有香味的液体,结合E的分子式可知,E为CH3COOCH2CH3,则B为CH3CH2OH,C为CH3CHO,D为CH3COOH,故A为CH2=CH2,乙烯发生加聚反应的F为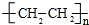 ,
,
(1)A为CH2=CH2,名称为乙烯,B为CH3CH2OH含有官能团为羟基,D为CH3COOH,含有官能团为羧基,故答案为:乙烯;CH2=CH2;羟基;羧基;
(2)反应②是乙醇催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,
反应⑤是乙烯发生加聚反应生成聚乙烯,反应方程式为: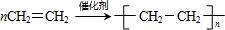 ,
,
故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,氧化反应; ,加聚反应.
,加聚反应.
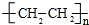 ,
,(1)A为CH2=CH2,名称为乙烯,B为CH3CH2OH含有官能团为羟基,D为CH3COOH,含有官能团为羧基,故答案为:乙烯;CH2=CH2;羟基;羧基;
(2)反应②是乙醇催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
| Cu |
| △ |
反应⑤是乙烯发生加聚反应生成聚乙烯,反应方程式为:
 ,
,故答案为:2CH3CH2OH+O2
| Cu |
| △ |
 ,加聚反应.
,加聚反应.
点评:本题考查有机物推断,涉及烯、醇、醛、羧酸之间的转化关系等,难度不大,注意基础知识的理解掌握.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、5.6g Fe投入100 mL 3.5mol?L-1稀硝酸中,充分反应,转移电子总数为0.3 NA |
| B、常温常压下,100g 17% H2O2水溶液含氧原子总数为NA |
| C、苯和苯甲酸混合物1 mol,完全燃烧消耗O2的分子数为7.5NA |
| D、2.24 L NH3中含共价键数目一定为0.3NA |
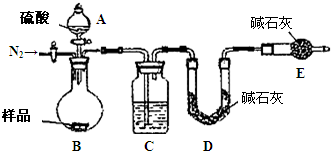 纯碱是工业生产和日常生活中的重要物质.某兴趣小组为测定某工业纯碱(假设仅含碳酸氢钠杂质)中碳酸钠的质量分数,设计了下列四种实验方案进行探究.请填空:
纯碱是工业生产和日常生活中的重要物质.某兴趣小组为测定某工业纯碱(假设仅含碳酸氢钠杂质)中碳酸钠的质量分数,设计了下列四种实验方案进行探究.请填空: