题目内容
下列说法正确的是( )
| A、强电解质溶液的导电性一定比弱电解质强 |
| B、医疗上血液的透析利用了胶体的性质,而用FeCl3紧急止血与胶体的性质无关 |
| C、氯水、氨水是混合物,盐酸是电解质,故盐酸是纯净物 |
| D、胶体与溶液的本质区别是分散质微粒的大小,可利用丁达尔现象区别溶液与胶体 |
考点:强电解质和弱电解质的概念,混合物和纯净物,分散系、胶体与溶液的概念及关系
专题:物质的分类专题
分析:A.电解质的强弱与电离程度有关,与溶液的导电性无关;
B.依据胶体的聚沉的性质解答;
C.电解质必须是化合物;
D.分散质微粒的大小是不同分散系划分的依据,丁达尔效应是胶体的特性.
B.依据胶体的聚沉的性质解答;
C.电解质必须是化合物;
D.分散质微粒的大小是不同分散系划分的依据,丁达尔效应是胶体的特性.
解答:
解:A.电解质的强弱与电离程度有关,与溶液的导电性无关,强电解质导电能力不一定强,故A错误;
B.血液是胶体,三氯化铁属于可溶性盐,能够是血液胶体聚沉,故B错误;
C.盐酸是氯化氢的水溶液,属于混合物,不是电解质,故C错误;
D.分散质微粒的大小是不同分散系划分的依据,分散质粒度小于1nm属于溶液,大于100nm属于浊液,介于1-100nm属于胶体,丁达尔效应是胶体的特性,可以用来鉴别胶体和溶液,故D正确;
故选:D.
B.血液是胶体,三氯化铁属于可溶性盐,能够是血液胶体聚沉,故B错误;
C.盐酸是氯化氢的水溶液,属于混合物,不是电解质,故C错误;
D.分散质微粒的大小是不同分散系划分的依据,分散质粒度小于1nm属于溶液,大于100nm属于浊液,介于1-100nm属于胶体,丁达尔效应是胶体的特性,可以用来鉴别胶体和溶液,故D正确;
故选:D.
点评:本题考查了强弱电解质的判断、胶体的性质,题目难度不大,明确相关概念和胶体性质是解题关键,注意对相关知识的积累.

练习册系列答案
相关题目
一定条件下,反应A+2B?2C在2L的容器中进行,5分钟内A的物质的量增加减少2mol,则在这段时间内用A表示的反应速率是( )
| A、0.1mol/(L.min) |
| B、2 mol/(L.min) |
| C、0.4 mol/(L.min) |
| D、0.2 mol/(L.min) |
茉莉醛具有浓郁的茉莉花香,其结构简式如图所示:关于茉莉醛的下列叙述错误的是( )
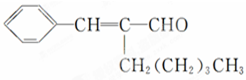
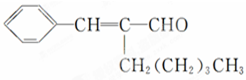
| A、在加热和催化剂作用下,能被氢气还原 |
| B、能被酸性高锰酸钾溶液氧化 |
| C、在一定条件下能与溴发生取代反应 |
| D、不能与氢溴酸发生加成反应 |
下列实验操作中错误的是( )
| A、分液时,先将分液漏斗中上层液体从上口倒出,再将下层液体从下口放出 |
| B、蒸馏时,温度计水银球处于蒸馏烧瓶的支管口附近 |
| C、使用容量瓶和分液漏斗前,要先检查是否漏水后再洗涤干净 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在称量纸上置于托盘天平的右盘中 |
室温下,pH=13的NaOH溶液与pH=2的H2SO4溶液混合,所得混合溶液pH=11,则NaOH溶液与H2SO4溶液的体积比为( )
| A、11:1 | B、9:1 |
| C、1:11 | D、1:9 |