题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、无色溶液中:H+、Na+、I-、ClO- |
| B、pH=13的溶液:Na+、K+、SiO32-、CO32- |
| C、含有较多Ag+溶液:HCO3-、K+、Na+、Cl- |
| D、c(H+)=0.1 mol?L-1的溶液:Na+、NH4+、SO42-、S2O32- |
考点:离子共存问题
专题:离子反应专题
分析:A.次氯酸根离子能够氧化碘离子、次氯酸根离子能够与氢离子结合生成次氯酸;
B.pH=13的溶液为碱性溶液,溶液中存在大量氢氧根离子,Na+、K+、SiO32-、CO32-离子之间不发生反应,都不与氢氧根离子反应;
C.银离子与氯离子生成氯化银沉淀;
D.S2O32-与氢离子发生反应生成二氧化硫气体和硫单质.
B.pH=13的溶液为碱性溶液,溶液中存在大量氢氧根离子,Na+、K+、SiO32-、CO32-离子之间不发生反应,都不与氢氧根离子反应;
C.银离子与氯离子生成氯化银沉淀;
D.S2O32-与氢离子发生反应生成二氧化硫气体和硫单质.
解答:
解:A.H+、ClO-之间反应生成次氯酸,I-、ClO-之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.pH=13的溶液中存在大量氢氧根离子,Na+、K+、SiO32-、CO32-之间不反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.Ag+、Cl-之间反应生成AgCl沉淀,在溶液中不能大量共存,故C错误;
D.S2O32-与溶液中氢离子反应生成二氧化硫气体和硫单质,在溶液中不能大量共存,故D错误;
故选B.
B.pH=13的溶液中存在大量氢氧根离子,Na+、K+、SiO32-、CO32-之间不反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.Ag+、Cl-之间反应生成AgCl沉淀,在溶液中不能大量共存,故C错误;
D.S2O32-与溶液中氢离子反应生成二氧化硫气体和硫单质,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的判断,为高考中的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、反应A(g)?2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ?mol-1,则△H=(Ea-Eb)kJ?mol-1 | ||
| B、标准状态下,将0.1 mol?L-1 的氨水溶液中加入少量氯化铵晶体,若混合溶液pH=7,则c(NH4+)=c(Cl-) | ||
| C、足量的锌铜合金与100mL pH=1 稀硫酸反应,反应3s 时测得pH=2,假设反应前后溶液的体积保持不变,则3s 内产生氢气的平均速率是33.6 mL?s-1 | ||
D、将浓度为0.1mol?L-1HF 溶液加水不断稀释过程中,电离度(α)和Ka(HF)保持不变,
|
影响化学反应速率的因素有多方面,如浓度.压强.温度.催化剂等.下列有关说法不正确的是( )
| A、改变压强能改变气体反应的速率 |
| B、增大浓度能加快化学反应速率,原因是增大浓度就增加了反应体系中活化分子的百分数 |
| C、温度升高使化学反应速率加快的主要原因是增加了反应体系中活化分子的百分数 |
| D、催化剂能加快化学反应速率主要原因是降低反应所需的能量 |
我们生活在千变万化的物质世界里.下列过程或变化中,没有发生氧化还原反应的是( )
| A、iPhone5手机电池充电 |
| B、铁制品镀铜 |
| C、爆竹爆炸 |
| D、利用焰色反应检验Na+ |
工业上进行下列物质的制取,其所示的物质的转化关系中,正确的是( )
A、以食盐为原料制Na2CO3:2NaCl+2H2O
| |||||||
B、以铜和硫酸为原料制取硫酸铜:2Cu+O2
| |||||||
| C、从海水中提取MgCl2:MgCl2+2NaOH=Mg(OH)2↓+2NaCl Mg(OH)2+2HCl=MgCl2+H2O | |||||||
D、黄铁矿为原料制硫酸:4FeS+7O2
|
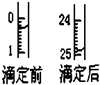 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.