题目内容
20.下列物质中,既含有离子键又含有共价键的是( )| A. | KOH | B. | LiCl | C. | H2 | D. | NH3 |
分析 一般来说,活泼金属元素与活泼非金属元素形成离子键,非金属元素之间形成共价键,以此来解答.
解答 解:A.钾离子和氢氧根之间是离子键,氢氧根内部存在共价键,故A正确;
B.氯化锂中只存在锂离子和氯离子之间的离子键,故B错误;
C.氢气中存在共价键,属于单质,故C错误;
D.氨气中只存在共价键,故D错误.
故选A.
点评 本题考查化学键,把握离子键、共价键判断的一般规律为解答的关键,注意特殊物质中的化学键(氯化铝、铵盐等),题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.对于化学反应3W(s)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
| A. | v(W)=3v(Z) | B. | 2v(X)=3v(Z) | C. | 2v(X)=v(Y) | D. | 2v(W)=3v(X) |
8.一个原电池反应是Zn+Cu2+=Zn2++Cu,该反应的原电池的组成正确的( )
| A | B | C | D | |
| 正极 | Zn | Ag | C | Cu |
| 负极 | Cu | Cu | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | CuSO4 | FeCl2 |
| A. | A | B. | B | C. | C | D. | D |
12.下列离子方程式书写正确的是( )
| A. | Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | |
| B. | 0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| C. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向FeI2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
9.下列反应最终无沉淀产生的是( )
| A. | 过量的CO2通入Na2SiO3溶液中 | |
| B. | 向AlCl3溶液中滴加稀氨水至过量 | |
| C. | 少量的CO2通入BaCl2溶液中 | |
| D. | 向FeCl3溶液中滴加NaOH溶液至过量 |
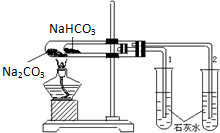 实验室利用如图所示装置进行Na2CO3和NaHCO3热稳定性对比实验.请回答:
实验室利用如图所示装置进行Na2CO3和NaHCO3热稳定性对比实验.请回答: