题目内容
将0.05mol某烃A完全燃烧后的产物先通过浓硫酸,浓硫酸增重4.5g;再通过碱石灰,碱石灰增重8.8g.求该烃的分子式,写出其可能的结构简式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:有机物燃烧产物通过浓硫酸,浓硫酸吸收水,增重4.5g,即生成4.5g的水,再通过碱石灰,碱石灰增重8.8g,即生成二氧化碳的质量是8.8g,根据生成水以及二氧化碳的质量结合计算碳原子和氢原子的数目,进而确定分子式和结构简式.
解答:
解:有机物燃烧产物通过浓硫酸,浓硫酸吸收水,增重4.5g,即生成4.5g的水,再通过碱石灰,碱石灰增重8.8g,即生成二氧化碳的质量是8.8g,设有机物的分子式为CxHy,
CxHy+
O2→
xCO2+
H2O
1mol 44x g 9y g
0.05mol 8.8g 4.5
解得x=4,y=10.
所以该烃的分子为C4H10,其可能的结构简式为CH3CH2CH2CH3和CH(CH3)3,答:该烃的分子为C4H10,其可能的结构简式为CH3CH2CH2CH3和CH(CH3)3.
CxHy+
| x+y |
| 4 |
| 点燃 |
| y |
| 2 |
1mol 44x g 9y g
0.05mol 8.8g 4.5
解得x=4,y=10.
所以该烃的分子为C4H10,其可能的结构简式为CH3CH2CH2CH3和CH(CH3)3,答:该烃的分子为C4H10,其可能的结构简式为CH3CH2CH2CH3和CH(CH3)3.
点评:本题考查学生燃烧法确定有机物分子式的方法,注意元素守恒思想的应用是关键,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、常温常压下,11.2L氯气所含的原子数为NA |
| B、常温常压下,1mol氦气含有的核外电子数为4NA |
| C、17g氨气所含的电子数目为10NA |
| D、同温同压下,相同体积的任何气体单质所含的原子数目相同 |
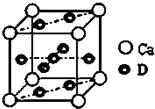 A,B,C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:
A,B,C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空: