题目内容
按要求填空: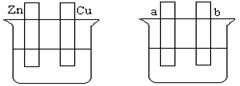
A B
(1)在A图中,稀硫酸为电解质溶液,用导线连接后,铜片电极反应式 。
(2)在B图中外接直流电源,若要在a极镀铜,加以必要的连接后,该装置叫 ,b极电极反应式 。
(3)在B图中外接直流电源,若电极为惰性电极,电解质溶液是CuSO4溶液(足量),电解总反应离子方程式为 ,阴极增重3.2 g,则阳极上放出的气体在标准状况下的体积是_____L,加入一定量的 后(填化学式),溶液能恢复至与电解前完全一致。
(1)2H+ +2e=H2↑
(2)电镀池或电镀,Cu - 2e- = Cu2+。
(3)2Cu2++2H2O 2Cu+O2↑+4H+ 0.56 CuO 。
2Cu+O2↑+4H+ 0.56 CuO 。
解析试题分析:(1)A反应为锌铜原电池,锌被氧化成Zn2+进入溶液,电子由锌片通过导线流向铜片,溶液中的H+从铜片获得电子,被还原成氢原子。氢原子结合成氢分子从铜片上放出。两极发生如下反应:负极:Zn-2e-=Zn2+ 正极: 2H+ +2e=H2↑ 铜片上的反应为:2H+ +2e=H2↑
(2)电镀的条件为:电源、电极、电解质、闭合回路,,而且题中指出要在a极镀铜,所以此装置为电镀池。要在a极镀铜,那么a极发生的是还原反应,b极发生的是氧化反应,电极反应方程式为:Cu - 2e- = Cu2+.
(3) 在B图中外接直流电源,若电极为惰性电极,电解质溶液是CuSO4溶液(足量),则此反应的离子反应方程式为2Cu2++2H2O 2Cu+O2↑+4H+,阴极反应方程式为:Cu2++2e-= Cu,又阴极增重3.2g,则增加铜的物质的量为0.05mol,则生成氧气的物质的量为0.05 mol/2="0.025" mol, 生成氧气的体积为0.025 mol×22.4L/ mol=0.56L。该反应析出了单质铜和氧气,根据元素守恒,应向其添加一定量的CuO,溶液能恢复至与电解前完全一致。
2Cu+O2↑+4H+,阴极反应方程式为:Cu2++2e-= Cu,又阴极增重3.2g,则增加铜的物质的量为0.05mol,则生成氧气的物质的量为0.05 mol/2="0.025" mol, 生成氧气的体积为0.025 mol×22.4L/ mol=0.56L。该反应析出了单质铜和氧气,根据元素守恒,应向其添加一定量的CuO,溶液能恢复至与电解前完全一致。
考点:本题着重考查了原电池、电解池、电镀池的相关知识。

 名校课堂系列答案
名校课堂系列答案某课外小组分别用下图所示装置对原电池和电解池原理进行实验探究。

图1 图2
请回答:
Ⅰ.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是 (填字母序号)。
| A.铝 | B.石墨 | C.银 | D.铂 |
(3)实验过程中,S
 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。
(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。 Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(Fe
 )在溶液中呈紫红色。
)在溶液中呈紫红色。(4)电解过程中,X极区溶液的pH (填“增大”“减小”或“不变”)。
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-
 Fe
Fe +4H2O和 。
+4H2O和 。 (6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况下的气体体积),则Y电极(铁电极)质量减少 g。
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:
2K2FeO4+3Zn
 Fe2O3+ZnO+2K2ZnO2
Fe2O3+ZnO+2K2ZnO2该电池正极发生的反应的电极反应为 。
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放109g5.51%的NaOH溶液、足量的CuSO4溶液和200g10.00%的K2SO4溶液.电极均为石墨电极。
接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
(1)电极b上发生的电极反应为___________________________________。
(2)电极b上生成的气体在标状况下的体积为__________________,此时甲烧杯中NaOH溶液的物质的量浓度为(设溶液的密度为1g/cm3)_______________。
(3)电极c的质量变化是___________g,欲使电解后乙中的电解液恢复到起始状态,应该向溶液中加入适量的___________(填字母编号)。
| A.Cu(OH)2 | B.Cu2O | C.CuCO3 | D.Cu2(OH)2CO3 |
某小组同学以碳棒为电极电解CuCl2溶液时,发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的产物,同学们阅读资料并设计了如下过程:
Ⅰ.有关资料:铜的化合物颜色性质如下
| 物质 | 颜色、性质 | 物质 | 颜色、性质 |
| 氢氧化铜Cu(OH)2 | 蓝色固体不溶于水 | 硫酸铜(CuSO4) | 溶液呈蓝色 |
| 氧化亚铜(Cu2O) | 红色固体不溶于水 | 氯化铜(CuCl2) | 浓溶液呈绿色,稀溶液呈蓝色 |
| 氯化亚铜(CuCl) | 白色固体不溶于水 | 碱式氯化铜 | 绿色固体不溶于水 |
Ⅱ.探究实验:
(1)提出假设
①红色物质一定有铜,还可能有Cu2O;
②白色物质为铜的化合物,其化学式可能为__________________________。
(2)实验验证
取电解CuCl2溶液后的阴极碳棒,洗涤、干燥,连接下列装置进行实验,验证阴极产物,
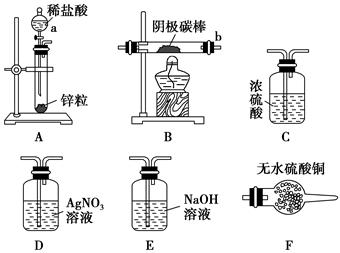
①实验前,检查装置A气密性的方法是_______________________________。
②实验时,各装置从左至右的连接顺序为A→________→________→B→________→________。
(3)观察现象,得出结论
实验结束后,碳棒上的白色物质变为红色,F中物质不变色,D中出现白色沉淀,根据现象①碳棒上的红色物质是否有Cu2O________(填“是”或“否”),理由是________________________________________________________;
②装置________(填上图中装置编号)中________的现象说明提出假设②中的白色物质一定存在;
③写出装置B中发生反应的化学方程式___________________________ _。
(4)问题讨论
①电解CuCl2溶液后的阴极上发生的反应为:______________________
和_______________________________________________________________;
②实验过程中,若装置B中的空气没有排净就开始加热,可能对实验造成的影响是__________________________________________________________。






