题目内容
实验室将9 g铝粉跟一定量的金属氧化物粉末混合形成铝热剂。发生铝热反应之后,所得固体中含金属单质为18 g,则该氧化物粉末可能是 ( )
A.Fe2O3和MnO2 B.MnO2和V2O5
C.Cr2O3和V2O5 D.Fe3O4和FeO
A、D
【解析】
试题分析: 9 g铝粉可以提供1 mol电子,则氧化物中的金属元素每得到1 mol电子对应的质量就应该是18 g。三价铁得到1 mol电子对应的质量为18.7 g,四价锰得到1 mol电子对应的质量为13.8 g,故A项正确。五价钒得到1 mol电子对应的质量为10.2 g,三价铬得到1 mol电子对应的质量为17.3 g,B、C两项,即使9 g铝粉全部反应,得到金属单质的质量也不到18 g,故都错误。Fe3O4中的铁元素得到1 mol电子对应的质量为21 g,FeO中二价铁得到1 mol电子对应的质量为28 g,当氧化物粉末不足时,D项正确。
考点:铝及铝合金

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目

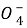 +5SO2+2H2O====2Mn2++5S
+5SO2+2H2O====2Mn2++5S +4H+
+4H+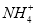 中,NH3发生氧化反应
中,NH3发生氧化反应