题目内容
下面是某同学在学习硫元素时的学习方案,请完善该同学的学习方案。
(1)硫原子的结构:硫原子的核内质子数为16,它的原子结构示意图是 ,从结构可以知道硫元素是一种典型的非金属元素。
(2)硫单质的物理性质:硫是一种淡黄色的 体(填“气”“液”或“固”),主要存在于火山喷发口附近或地壳的岩层里,这是硫以游离态形式存在于自然界中。硫元素在自然界中也有以化合态形式存在的,如许多金属矿石是含硫化合物,如胆矾 (填化学式)。
(3)设计如下实验探究硫和含硫化合物的相互转化:
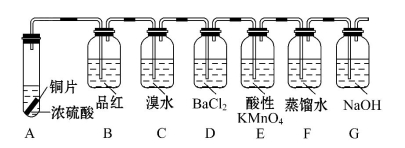
(Ⅰ)完成下列各个反应的化学方程式
①A中在加热时发生的反应
。
②C中的反应
。
(Ⅱ)记录观察到的实验现象
①B中品红溶液由红色变为 ,加热后又 ,(结论:可以根据该现象用品红溶液来证明SO2的存在与否)。
②D中没有观察到什么现象,在实验结束后往D中滴加H2O2后则可以看到 。
③E中溶液由紫红色变为无色,反应的离子方程式是
2Mn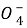 +5SO2+2H2O====2Mn2++5S
+5SO2+2H2O====2Mn2++5S +4H+
+4H+
反应中SO2是 剂(填“氧化”或“还原”)。
(Ⅲ)G的作用是吸收尾气,写出反应的离子方程式:
。
(1)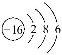 (2)固 CuSO4·5H2O (3)(Ⅰ)①Cu+2H2SO4(浓)
(2)固 CuSO4·5H2O (3)(Ⅰ)①Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
②Br2+SO2+2H2O====2HBr+H2SO4 (Ⅱ)①无色 变红 ②白色浑浊现象 ③还原
(Ⅲ)SO2+2OH-====S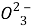 +H2O
+H2O
【解析】
试题分析:铜和浓硫酸在加热条件下反应生成CuSO4、SO2和H2O,SO2是一种酸性氧化物(能够和水、碱、碱性氧化物、某些酸性比亚硫酸弱的弱酸盐反应),它既有氧化性(能够将H2S氧化成硫沉淀),又有还原性(能够被溴水、酸性高锰酸钾溶液、双氧水、氧气等强氧化性物质氧化成SO3、H2SO4等含+6价硫元素的物质),还有漂白性(能够使品红溶液褪色,生成的无色物质不稳定,加热后又变红)。
考点:硫酸的制备和性质

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案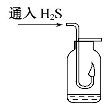
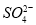 ,你认为合理的是 ( )
,你认为合理的是 ( ) 白色沉淀
白色沉淀 沉淀不溶解
沉淀不溶解 无沉淀
无沉淀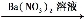 白色沉淀
白色沉淀