题目内容
现有镁铝合金共3.9克,与500 mL 2 mol·L-1盐酸(足量)反应,生成的气体在标准状况下体积为4.48 L,若反应后所得溶液的体积仍为500 mL,求:
(1)镁铝合金中铝的物质的量。
(2)镁铝合金中镁的质量分数。
(3)反应后溶液中Cl-的物质的量浓度。
(1)0.1 mol (2)30.8% (3)2 mol·L-1
【解析】
试题分析:(1)4.48 L氢气的物质的量为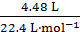 =0.2 mol,令金属中Mg的物质的量为xmol、Al的物质的量为ymol,则:
=0.2 mol,令金属中Mg的物质的量为xmol、Al的物质的量为ymol,则:
Mg+2HCl====MgCl2+H2↑,
xmol xmol
2Al+6HCl====2AlCl3+3H2↑
ymol 1.5ymol
所以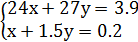 ,解得:x=0.05,y=0.1
,解得:x=0.05,y=0.1
(2)3.9 g合金中Mg的质量为0.05 mol×24 g·mol-1=1.2 g,镁铝合金中镁的质量分数=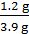 ×100%=30.8%;(3)Cl-没有参加反应,Cl-浓度不变,等于开始盐酸的浓度,故c(Cl-)=2 mol·L-1。
×100%=30.8%;(3)Cl-没有参加反应,Cl-浓度不变,等于开始盐酸的浓度,故c(Cl-)=2 mol·L-1。
考点:铝及铝合金

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
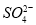 ,你认为合理的是 ( )
,你认为合理的是 ( ) 白色沉淀
白色沉淀 沉淀不溶解
沉淀不溶解 无沉淀
无沉淀 白色沉淀
白色沉淀