题目内容
化学在日常生活和生产中有着重要的应用.下列说法不正确的有( )
①明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化;
②生活中常用苏打作发酵粉;
③在海轮外壳上镶入锌块,可减缓船体的腐蚀速率;
④燃煤时加入适量石灰石,可减少废气中SO2的量;
⑤高温下浓硫酸可以用铁制容器盛放;
⑥工业上常用硅制造光导纤维.
①明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化;
②生活中常用苏打作发酵粉;
③在海轮外壳上镶入锌块,可减缓船体的腐蚀速率;
④燃煤时加入适量石灰石,可减少废气中SO2的量;
⑤高温下浓硫酸可以用铁制容器盛放;
⑥工业上常用硅制造光导纤维.
| A、1个 | B、2个 | C、3个 | D、4个 |
考点:盐类水解的应用,金属的电化学腐蚀与防护,浓硫酸的性质,硅和二氧化硅,钠的重要化合物
专题:元素及其化合物,化学应用
分析:①胶体能吸附水中悬浮物而净水;
②生活中常用小苏打作发酵粉;
③作原电池正极的金属被保护;
④高温下,二氧化硫和氧化钙反应生成亚硫酸钙;
⑤高温下浓硫酸和铁发生氧化还原反应;
⑥工业上常用二氧化硅制造光导纤维,
②生活中常用小苏打作发酵粉;
③作原电池正极的金属被保护;
④高温下,二氧化硫和氧化钙反应生成亚硫酸钙;
⑤高温下浓硫酸和铁发生氧化还原反应;
⑥工业上常用二氧化硅制造光导纤维,
解答:
解:①明矾水解形成的Al(OH)3胶体能吸附水中悬浮物而净水,所以明矾可用于水的净化,故正确;
②小苏打具有碱性且碱性较弱,生活中常用小苏打作发酵粉,中和酸,故错误;
③在海轮外壳上镶入锌块,Fe、Zn和海水构成原电池,锌易失电子作负极,Fe作正极被保护,所以在海轮外壳上镶入锌块可减缓船体的腐蚀速率,故正确;
④燃煤时加入适量石灰石,石灰石高温下分解生成CaO,CaO和二氧化硫生成亚硫酸钙,所以可减少废气中SO2的量,故正确;
⑤高温下浓硫酸和铁发生氧化还原反应生成二氧化硫,所以不可以用铁制容器盛放,常温下铁和浓硫酸发生钝化现象,所以常温下,铁容器能盛放浓硫酸,故错误;
⑥工业上常用二元化硅制造光导纤维,硅能制造硅芯片和太阳能电池,故错误;
故选C.
②小苏打具有碱性且碱性较弱,生活中常用小苏打作发酵粉,中和酸,故错误;
③在海轮外壳上镶入锌块,Fe、Zn和海水构成原电池,锌易失电子作负极,Fe作正极被保护,所以在海轮外壳上镶入锌块可减缓船体的腐蚀速率,故正确;
④燃煤时加入适量石灰石,石灰石高温下分解生成CaO,CaO和二氧化硫生成亚硫酸钙,所以可减少废气中SO2的量,故正确;
⑤高温下浓硫酸和铁发生氧化还原反应生成二氧化硫,所以不可以用铁制容器盛放,常温下铁和浓硫酸发生钝化现象,所以常温下,铁容器能盛放浓硫酸,故错误;
⑥工业上常用二元化硅制造光导纤维,硅能制造硅芯片和太阳能电池,故错误;
故选C.
点评:本题考查物质的用途,明确物质的性质是解本题关键,注意:高温和常温下,铁与浓硫酸反应现象的区别,为易错点.

练习册系列答案
相关题目
根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )
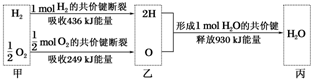

| A、H2O分解为H2与O2时放出热量 |
| B、生成1mol H2O时吸收热量245kJ |
| C、氢气和氧气的总能量小于水的能量 |
| D、甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙 |
下列叙述正确的是( )
| A、25℃时,0.1mol/L的醋酸中,c(H+)=0.1mol/L | ||
| B、在稀醋酸溶液中加入少量醋酸钠固体,会促进醋酸的电离 | ||
| C、在稀氨水中通入氨气,所得溶液的pH减小 | ||
D、向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中
|
下列实验方法或操作正确的是( )
| A、用标准氢氧化钠溶液滴定待测醋酸,选用酚酞作指示剂 |
| B、配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再加水稀释到所需的浓度 |
| C、测定某溶液的pH时,用pH试纸蘸取待测液,然后和比色卡对比得出pH |
| D、将淀粉溶液加到饱和食盐水中,检验食盐是否是加碘食盐 |
2011年3月11日,日本本州岛仙台港发生9.0级地震,地震引发海啸、食盐、蔗糖、醋酸、“84消毒液”、明矾等是灾后居民日常生活中经常使用的物质,下列有关说法或表示正确的是( )
A、食盐中阴离子的结构示意图为: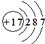 |
| B、蔗糖和醋酸都是弱电解质 |
C、“84消毒液”中有效成分NaClO的电子式为: |
| D、明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒 |
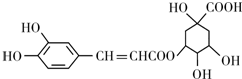
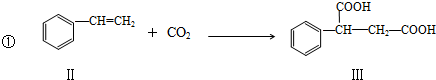
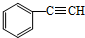 和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应,Ⅵ和Ⅶ的结构简式分别为
和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应,Ⅵ和Ⅶ的结构简式分别为