题目内容
常用两种方法制备氯化物:①金属与氯气直接化合;②金属与盐酸反应.用上述两种方法都可制得的氯化物是( )
| A、CuCl2 |
| B、FeCl2 |
| C、FeCl3 |
| D、AlCl3 |
考点:氯气的化学性质,常见金属元素的单质及其化合物的综合应用
专题:元素及其化合物
分析:Al、Mg为活泼金属,可与盐酸或氯气都能反应,因化合价唯一,则生成物唯一,Fe为变价金属,与盐酸反应生成FeCl2,与氯气反应生成FeCl3,Cu与盐酸不反应,以此解答.
解答:
解:A.Cu与盐酸不反应,故A错误;
B.Fe和氯气直接化合制得FeCl3,但Fe与稀盐酸反应生成FeCl2,不符合题意,故B错误;
C.Fe与稀盐酸反应生成FeCl2,不能得到FeCl3,故C错误;
D.Al和氯气直接化合制得AlCl3,且Al与盐酸反应制得AlCl3,符合题意,故D正确.
故选D.
B.Fe和氯气直接化合制得FeCl3,但Fe与稀盐酸反应生成FeCl2,不符合题意,故B错误;
C.Fe与稀盐酸反应生成FeCl2,不能得到FeCl3,故C错误;
D.Al和氯气直接化合制得AlCl3,且Al与盐酸反应制得AlCl3,符合题意,故D正确.
故选D.
点评:本题考查物质的制备,侧重于元素化合物知识的考查,为高频考点,明确铁、氯气、盐酸的性质及发生的化学反应是解答本题的关键,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
用惰性电极电解下列溶液一段时间后,再加入一定量的某种纯净物(括号内物质),不能使溶液恢复到原来的成分和浓度的是( )
| A、KCl(HCl) |
| B、H2SO4(H2O) |
| C、AgNO3(HNO3) |
| D、CuSO4(CuCO3) |
在下列反应中,水仅作还原剂的是( )
| A、Na2O+H2O=2NaOH |
| B、2F2+2H2O=4HF+O2 |
| C、Cl2+H2O=HCl+HClO |
| D、2K+2H2O=2KOH+H2↑ |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4LCCl4含有的分子数为NA |
| B、标准状况下,3.2g氧气(O2)和臭氧(O3)中含有的分子总数为0.1NA |
| C、含4molHCl的浓盐酸与足量的MnO2反应,转移电子总数为2NA |
| D、常温下,78gNa2O2中含有的阴离子数是NA |
漂白粉长期露置在空气中失效的原因是( )
| A、吸收了氧气和水蒸气 |
| B、吸收了二氧化碳和水蒸气 |
| C、漂白粉风化 |
| D、漂白粉不稳定,见光分解 |
燃料充分燃烧的条件是( )
| A、有更高的温度 |
| B、有氧气参加 |
| C、达到着火点 |
| D、与空气有足够大的接触面 |
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图: | ||
B、H2O的电子式: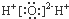 | ||
C、原子核内有10个中子的氧原子:
| ||
D、CO2的比例模型: |