题目内容
物质的量相等的CO和CO2相比较,下列有关叙述中正确的是( )
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们所含的电子数目之比为7:11.
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们所含的电子数目之比为7:11.
| A、①和④ | B、②和③ |
| C、①②③④ | D、①②③④⑤ |
考点:阿伏加德罗定律及推论
专题:计算题,阿伏加德罗常数和阿伏加德罗定律
分析:根据N=nNA计算微粒数目.
①物质的量相同,分子数相同;
②1个CO和CO2分子中所含氧原子数分别为1个、2个;
③1个CO和CO2分子中所含原子数分别为2个、3个;
④1个CO和CO2分子中所含碳原子数都是1个;
⑤CO和CO2分子中所含电子数分别为14个、22个.
①物质的量相同,分子数相同;
②1个CO和CO2分子中所含氧原子数分别为1个、2个;
③1个CO和CO2分子中所含原子数分别为2个、3个;
④1个CO和CO2分子中所含碳原子数都是1个;
⑤CO和CO2分子中所含电子数分别为14个、22个.
解答:
解:①由于N=nNA,所以物质的量相同,分子数相同,故①正确;
②CO和CO2分子中所含氧原子数分别为1个、2个,相等物质的量的CO和CO2所含氧原子的物质的量之比为1:2,由于N=nNA,所含氧原子数之比为1:2,故②正确;
③CO和CO2分子中所含原子数分别为2个、3个,相等物质的量的CO和CO2所含原子的物质的量之比为2:3,由于N=nNA,所含原子数之比为2:3,故③正确;
④CO和CO2分子中所含碳原子数都是1个,相等物质的量的CO和CO2所含碳原子的物质的量之比为1:1,由于N=nNA,所含碳原子数之比为1:1,故④正确;
⑤CO和CO2分子中所含电子数分别为14个、22个,相等物质的量的CO和CO2所含电子的物质的量之比为14:22=7:11,由于N=nNA,所含电子数之比为7:11,故⑤正确.
故选D.
②CO和CO2分子中所含氧原子数分别为1个、2个,相等物质的量的CO和CO2所含氧原子的物质的量之比为1:2,由于N=nNA,所含氧原子数之比为1:2,故②正确;
③CO和CO2分子中所含原子数分别为2个、3个,相等物质的量的CO和CO2所含原子的物质的量之比为2:3,由于N=nNA,所含原子数之比为2:3,故③正确;
④CO和CO2分子中所含碳原子数都是1个,相等物质的量的CO和CO2所含碳原子的物质的量之比为1:1,由于N=nNA,所含碳原子数之比为1:1,故④正确;
⑤CO和CO2分子中所含电子数分别为14个、22个,相等物质的量的CO和CO2所含电子的物质的量之比为14:22=7:11,由于N=nNA,所含电子数之比为7:11,故⑤正确.
故选D.
点评:本题考查常用化学计量的有关计算、阿伏伽德罗定律及推论,题目难度不大,注意有关公式的利用与影响气体体积的因素.

练习册系列答案
相关题目
常用两种方法制备氯化物:①金属与氯气直接化合;②金属与盐酸反应.用上述两种方法都可制得的氯化物是( )
| A、CuCl2 |
| B、FeCl2 |
| C、FeCl3 |
| D、AlCl3 |
下列离子方程式正确的是( )
| A、过量氯气通入碘化亚铁溶液中:Cl2+Fe2++2I-=2Cl-十Fe3++I2 |
| B、向NaHCO3溶液中加入少量澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
| C、H218O中投入少量Na2O2固体:2H218O+2 Na2O2=4Na++4OH-+18O2↑ |
| D、向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
橄榄石型LiFePO4是以中国锂离子电池正极材料,下列有关LiFePO4的说法中不正确的是( )
| A、LiFePO4中铁元素的化合价为+2价 |
| B、LiFePO4中Li、P、O均属于短周期元素 |
| C、能与稀硝酸发生氧化还原反应 |
| D、LiFePO4中Li、Fe、P均属于主族元素 |
下列说法中错误的是( )
| A、同一元素的各种同位素的化学性质相似 |
| B、元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
| C、除氦外的稀有气体原子的最外层电子数都是8 |
| D、原子及其离子的核外电子层数等于该元素所在的周期数 |
同温同压下,下列气体的密度最大的是( )
| A、F2 |
| B、Cl2 |
| C、HCl |
| D、CO2 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是(相对原子量:H-1 C-12)( )
| A、1 mol/L氯化铜溶液中的Cu2+数小于NA |
| B、标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA |
| C、常温常压下,16g氧气和16g臭氧(O3)所含有的氧原子数均为NA |
| D、1 mol CH5+所含电子数为8NA |
能正确表示下列反应的离子方程式为( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C、碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
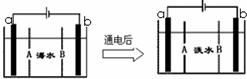 电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是
电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是