题目内容
16.某有机物A的结构简式为HOOC-CH═CH-CH2OH(1)请你写出该有机物官能团的名称:羟基、羧基、碳碳双键
(2)验证该有机物中含有-COOH官能团常采用的方法碳酸钠溶液或石蕊试液,产生的现象为产生气泡或变红
(3)写出下列反应的化学方程式,并注明反应类型.
①A和溴水反应HOOC-CH═CH-CH2OH+Br2→HOOC-CHBr-CHBr-CH2OH,加成反应
②A和乙酸反应HOOC-CH═CH-CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH=CHCOOH+H2O,酯化反应
③A和乙醇反应HOOC-CH═CH-CH2OH+CH3CH2OH$→_{△}^{浓硫酸}$CH2OHCH=CHCOOCH2CH3+H2O,酯化反应.
分析 (1)根据有机物的结构特点判断有机物含有的官能团;
(2)羧基具有酸的通性:使石蕊试液变红、能和碳酸钠反应生成二氧化碳等;
(3)有机物HOOC-CH═CH-CH2OH中含有碳碳双键,能够与溴水发生加成反应,含有羟基,能够与乙酸发生酯化反应,含有羧基,能够与乙醇发生酯化反应,分别写出反应的化学方程式.
解答 解:(1)根据有机物的结构简式可知,该有机物含有羟基、羧基、碳碳双键三种官能团,
故答案为:羟基、羧基、碳碳双键;
(2)羧基具有酸的通性,能使石蕊试液变红,能和碳酸钠反应生成二氧化碳等,所以可用碳酸钠溶液或石蕊试液验证,
故答案为:碳酸钠溶液或石蕊试液;产生气泡或变红;
(1)①HOOC-CH═CH-CH2OH分子中含有碳碳双键,能够与溴水发生加成反应,反应的化学方程式为:HOOC-CH═CH-CH2OH+Br2→HOOC-CHBr-CHBr-CH2OH,
故答案为:HOOC-CH═CH-CH2OH+Br2→HOOC-CHBr-CHBr-CH2OH,加成反应;
②HOOC-CH═CH-CH2OH分子中含有羟基,能够与乙酸发生酯化反应,反应的化学方程式为:HOOC-CH═CH-CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH=CHCOOH+H2O,
故答案为:HOOC-CH═CH-CH2OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH=CHCOOH+H2O,酯化反应;
③HOOC-CH═CH-CH2OH分子中含有羧基,能够与乙醇发生酯化反应,反应的化学方程式为:HOOC-CH═CH-CH2OH+CH3CH2OH$→_{△}^{浓硫酸}$CH2OHCH=CHCOOCH2CH3+H2O,
故答案为:HOOC-CH═CH-CH2OH+CH3CH2OH$→_{△}^{浓硫酸}$CH2OHCH=CHCOOCH2CH3+H2O,酯化反应.
点评 本题考查了有机物结构与性质,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握常见有机反应类型及判断方法,能够正确书写常见有机反应方程式.

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案| A. | Na+ H+ Cl- NO3- | B. | Na+ Mg2+ Cl- SO42- | ||
| C. | K+ Ba2+ OH- I- | D. | K+ OH- Br- Cl- |
| A. | 氧化钠可用于呼吸面具中作为氧气的来源 | |
| B. | 氧化还原反应的实质是元素化合价是否变化 | |
| C. | 铁制容器可以贮运稀硝酸 | |
| D. | 雷电为自然界固氮提供了条件 |
 已知氮元素有多种化合价,如:-3、0、+1、+2、+3、+4、+5.
已知氮元素有多种化合价,如:-3、0、+1、+2、+3、+4、+5.(1)下表是硝酸与某种金属M在某些条件下反应所得还原产物的关系:
| 硝酸 | 硝酸浓度大于10mol/L | 硝酸浓度为6.6~10mol/L、加热 | 硝酸浓度为6.6~10mol/L |
| 还原产物 | NO2 | NO2 | NO2 |
| 硝酸 | 硝酸浓度为0.1~6.6mol/L、加热 | 硝酸浓度0.1~6.6mol/L | 硝酸浓度0.1mol/L |
| 还原产物 | NO | NO2、N2 | NH4NO3 |
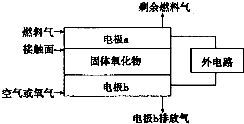
(2)以氨作为燃料的固体氧化物(含有O2-,接触面可让O2-通过)燃料电池,具有全固态结构、能量效率高、无污染等特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体.其工作原理如图所示
①负极为a(选填“a”或“b”).
②该电池工作时的总反应为4NH3+3O2=2N2+6H2O.
③固体氧化物作为电池工作的电解质,O2-移动方向为由电极b向电极a移动(选填“由电极a向电极b”或“由电极b向电极a”).
④该电池工作时,在图中所给的接触面上发生的电极反应为:2NH3+3O2--6e-=N2+3H2O.
| A. | 臭氧消毒 | B. | 丹桂飘香 | C. | 牛奶变酸 | D. | 食醋除锈 |
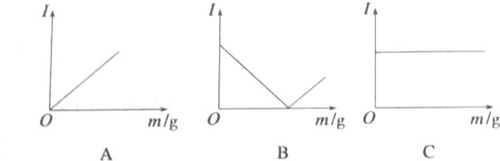
 某温度下,固体溶质之溶解度曲线如右图,试依据此图回答下列问题:
某温度下,固体溶质之溶解度曲线如右图,试依据此图回答下列问题: