题目内容
某同学用如图所示装置进行铜的电解精炼实验(粗铜中有锌、铁、镍、银等杂质,部分导线未画出),下列说法正确的是( )


| A、a应与c相连接,b应与d相连接 |
| B、电解一段时间,b与d两极析出物质的物质的量相等 |
| C、电解一段时间,b极附近溶液的pH降低 |
| D、电解过程中,Y装置中Cu2+的浓度始终不变 |
考点:原电池和电解池的工作原理
专题:
分析:X为原电池Y为电解池,X池中Zn为负极接Y池的纯铜,Cu为正极接Y池的粗铜,X中a极电极反应式为Zn-2e-=Zn2+,b极电极反应式为2H++2e-=H2↑,Y池中c极电极反应式为:Zn-2e-=Zn2+,Fe-2e-=Fe2+,Cu-2e-=Cu2+,d极电极反应式为Cu2++2e-=Cu,据此解答.
解答:
解:A、X池中Zn为负极接Y池的纯铜,Cu为正极接Y池的粗铜,故A错误;
B、b极电极反应式为2H++2e-=H2↑,d极电极反应式为Cu2++2e-=Cu,所以电解一段时间后,bd两极析出物质的物质的量相同,故B正确;
C、b极电极反应式为2H++2e-=H2↑,电解后pH升高,故C错误;
D、Y池中c极电极反应式为:Zn-2e-=Zn2+,Fe-2e-=Fe2+,Cu-2e-=Cu2+,d极电极反应式为Cu2++2e-=Cu,故D错误;
故选B.
B、b极电极反应式为2H++2e-=H2↑,d极电极反应式为Cu2++2e-=Cu,所以电解一段时间后,bd两极析出物质的物质的量相同,故B正确;
C、b极电极反应式为2H++2e-=H2↑,电解后pH升高,故C错误;
D、Y池中c极电极反应式为:Zn-2e-=Zn2+,Fe-2e-=Fe2+,Cu-2e-=Cu2+,d极电极反应式为Cu2++2e-=Cu,故D错误;
故选B.
点评:本题考查原电池和电解池相关知识,注意放电顺序.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列垃圾中,不适合用卫生填埋、焚烧、堆肥等处理方法处理的是( )
| A、电池 | B、农用塑料薄膜 |
| C、卫生纸 | D、纯棉纺织品 |
下列是关于氯水的叙述,正确的是( )
| A、新制氯水中只含C12和HClO分子 |
| B、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| C、光照氯水有气泡冒出,该气体为Cl2 |
| D、氯水放置数天后,pH值将增大 |
下列说法正确的是( )
| A、不溶于水的物质的溶解度为0 |
| B、H+与OH-在水溶液中混合时,反应的活化能几乎为0 |
| C、对已达平衡的可逆反应,v(正)=v(逆)=0 |
| D、常温下,1mol/L的CH3COOH溶液,pH=0 |
下列实验操作中,正确的是( )
| A、在容量瓶中直接溶解氢氧化钠固体 |
| B、向试管中滴加试剂时,将滴管下端紧靠试管内壁 |
| C、使用试纸检验溶液的性质时,将试纸浸入溶液中 |
| D、倾倒液体时试剂瓶标签向手心 |
下列水解的离子方程式正确的是( )
| A、S2-+2H2O?H2S+2OH- |
| B、Fe3++3H2O?Fe(OH)3+3H+ |
| C、HCO3-+H2O?CO32-+H3O+ |
| D、HS-+H2O?H2S↑+OH- |
下列化学用语表达正确的是( )
A、S2-的结构示意图: |
B、NaCl的电子式: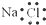 |
| C、Cl2的结构式:Cl-Cl |
| D、NaHCO3的电离方程式:NaHCO3=Na++H++CO32- |