题目内容
已知反应:3Cl2+8NH3═N2+6NH4Cl
(1)参加反应的NH3和作为还原剂的NH3的个数比为多少?
(2)若标准状况下33.6LCl2参加反应则被氧化的NH3的质量为多少?将还原产物溶于水配成500ml溶液其物质的量浓度为多少?(有计算步骤)
(1)参加反应的NH3和作为还原剂的NH3的个数比为多少?
(2)若标准状况下33.6LCl2参加反应则被氧化的NH3的质量为多少?将还原产物溶于水配成500ml溶液其物质的量浓度为多少?(有计算步骤)
考点:氧化还原反应的计算
专题:
分析:(1)该反应3Cl2+8NH3═N2+6NH4Cl中Cl元素化合价由0价变为-1价、N元素化合价由-3价变为0价,所以氯气是氧化剂,氨气是还原剂;
(2)根据氮原子守恒计算被氧化的氨气质量,根据c=
计算溶液的物质的量浓度.
(2)根据氮原子守恒计算被氧化的氨气质量,根据c=
| n |
| V |
解答:
解:(1)该反应8NH3+3Cl2=6NH4Cl+N2 中Cl元素化合价由0价变为-1价、N元素化合价由-3价变为0价,所以氯气是氧化剂、部分氨气是还原剂,作还原剂的氨气是2mol,参加反应的氨气是8mol,所以参加反应的NH3和作为还原剂的NH3的个数比为8:2=4:1,答:参加反应的NH3和作为还原剂的NH3的个数比为4:1;
(2)若标准状况下33.6LCl2参加反应,n(Cl2)=
=1.5mol,根据氮原子守恒知,参加反应的氯气是3mol时,被氧化的NH3是2mol,所以当参加反应的氯气时1.5moL,则被氧化的NH3的物质的量是1mol,质量是17g,
根据反应得到:3Cl2→6NH4Cl,设生成氯化铵的物质的量是n,
3Cl2→6NH4Cl
3mol 6mol
1.5mol n
得n=3mol,则c(NH4Cl)=
=6mol/L,
答:被氧化的NH3的质量是17g,溶液中氯化铵的物质的量浓度为6mol/L.
(2)若标准状况下33.6LCl2参加反应,n(Cl2)=
| 33.6L |
| 22.4L/mol |
根据反应得到:3Cl2→6NH4Cl,设生成氯化铵的物质的量是n,
3Cl2→6NH4Cl
3mol 6mol
1.5mol n
得n=3mol,则c(NH4Cl)=
| 3mol |
| 0.5L |
答:被氧化的NH3的质量是17g,溶液中氯化铵的物质的量浓度为6mol/L.
点评:本题考查了氧化还原反应,明确元素化合价变化是解本题关键,结合基本概念来分析解答,注意采用原子守恒即可解答,注意只有部分氨气作还原剂,为易错点.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
已知室温时,0.1mol/L某一元酸HA,PH=4,下列说法正确的是( )
| A、HA在水中有0.001%发生电离 |
| B、HA的电离平衡常数K=10-8mol/L |
| C、升高温度时,PH增大 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列有机物不是同一种物质的是( )
A、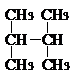 与 与 |
B、 与新戊烷 与新戊烷 |
C、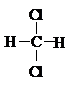 与 与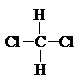 |
| D、C(CH3)3C(CH3)3与CH3(CH2)3C(CH3)3 |
某温度下,反应H2(g)+I2(g) 2HI(g);△H>0.在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
| A、恒温,压缩体积,平衡不移动,混合气体颜色加深 |
| B、恒压,充入HI(g),开始时正反应速率减小 |
| C、恒容,升高温度,逆反应速率减小 |
| D、恒容,充入H2,再次达到平衡时H2(g)的体积分数增大 |
下列物质是非电解质的是( )
| A、CO2 |
| B、AgCl |
| C、Cu |
| D、氨水 |
下列叙述错误的是( )
| A、生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B、用锡焊接的铁质器件,焊接处易生锈 |
| C、在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 |
| D、电解精炼铜时,电解质溶液中铜离子浓度减小 |
学校餐厅内长期使用不锈钢餐具,它也不会生锈的原因是在炼钢的过程中加入了下列物质的( )
| A、铬、锰 | B、铬、硅 |
| C、铬、镍 | D、铬、碳 |
某同学用如图所示装置进行铜的电解精炼实验(粗铜中有锌、铁、镍、银等杂质,部分导线未画出),下列说法正确的是( )


| A、a应与c相连接,b应与d相连接 |
| B、电解一段时间,b与d两极析出物质的物质的量相等 |
| C、电解一段时间,b极附近溶液的pH降低 |
| D、电解过程中,Y装置中Cu2+的浓度始终不变 |
关于NaOH溶液和Fe(OH)3胶体描述正确的是( )
| A、两者的分散质都属于碱 |
| B、两者均为有色不透明的分散系 |
| C、两者分散质的直径都介于10-9~10-7m之间 |
| D、一束光线分别通过时,两者都会产生“丁达尔效应” |