题目内容
19.下面图(1)和图(2)是A、B两种物质的核磁共振氢谱.已知A、B两种物质都是烃类,都含有6个氢原子.请根据图(1)和图(2)两种物质的核磁共振氢谱图选择出可能属于图(1)和图(2)的两种物质( )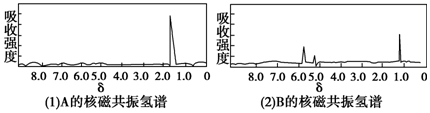
| A. | A是C3H8;B是C6H6 | B. | A是C4H10;B是C6H6 | ||
| C. | A是C3H6;B是C3H6 | D. | A是C3H6;B是C2H6 |
分析 A、B两种物质都是烃类,都含有6个氢原子,结合图中核磁共振氢谱可知,A中含1种H,B中含3种H,以此来解答.
解答 解:A、B两种物质都是烃类,都含有6个氢原子,C3H8、C4H10中H原子数分别为8、10,可排除选项A、B,
C3H6若为环丙烷,只含1种H,若为CH3CH=CH2,含3种H,符合,而C2H6中含1种H,
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物H原子及核磁共振氢谱图为解答的关键,侧重分析与应用能力的考查,注意同分异构体的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 18 g D2O和18 g H2O中含有的质子数均为10 NA | |
| B. | 22.4 LC02中含有共价键数目4 NA | |
| C. | 若H2O2分解产生成0.1mol氧气转移的电子数为0.2 NA | |
| D. | 同温、同压同体积的CO和NO含有的电子数相等 |
10.二氧化碳重整甲烷不仅可以获得合成气(CO和H2)还可减少温室气体排放.回答下列问题:
(1)已知断裂1mol化学键所需的能量如表:(CO的化学键近似表示为CO):
则反应CH4(g)+CO2(g)?2CO(g)+2H2(g)△H=+238KJ/molkJ•mol-1.
(2)在T℃时,向恒温4L的密闭容器中通入6mol CO2、6mol CH4,在催化剂作用下发生反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).达平衡时H2的体积分数为0.4,若再向容器中同时充入2mol CO2、6molCH4、4molCO和8molH2,则上述平衡向逆反应(填“正反应”或“逆反应”)方向移动.
(3)CH4/CO2重整反应通过热力学计算可得到的图象之一如图1.实际生产中有C、H2O(g)等生成,生成碳的反应之一为CH4(g)?C(s)+2H2(g),600℃之后,C的物质的量减少,请用方程式表示C减少的原因C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO.
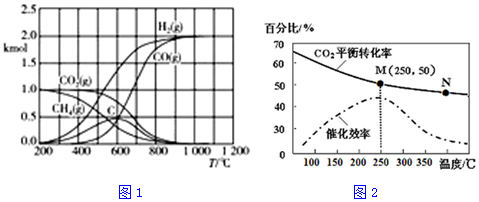
(4)不同温度对CO2的转化率及催化剂的效率影响如图2所示,下列有关说法不正确的是①②④(填序号).
①不同条件下反应,N点的速率最大
②温度低于250℃时,随温度升高乙烯的产率增大
③M点时平衡常数比N点时平衡常数大
④实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)已知某温度下CO2(g)+CH4(g)?2CO(g)+2H2(g)的平衡常数为K1
H2O(g)+CH4(g)?CO(g)+3H2(g)的平衡常数为K2
C(s)+H2O(g)?2CO(g)+2H2(g)的平衡常数为K3
则反映C(g)+CO2(g)?2CO(g) 的平衡常数为K为$\frac{{K}_{3}{•K}_{1}}{{K}_{2}}$(用K1、K2、K3表示)
(1)已知断裂1mol化学键所需的能量如表:(CO的化学键近似表示为CO):
| 化学键 | C≡O | C=O | C-H | H-H |
| 能量/kJ•mol-1 | 1074 | 803 | 413 | 436 |
(2)在T℃时,向恒温4L的密闭容器中通入6mol CO2、6mol CH4,在催化剂作用下发生反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).达平衡时H2的体积分数为0.4,若再向容器中同时充入2mol CO2、6molCH4、4molCO和8molH2,则上述平衡向逆反应(填“正反应”或“逆反应”)方向移动.
(3)CH4/CO2重整反应通过热力学计算可得到的图象之一如图1.实际生产中有C、H2O(g)等生成,生成碳的反应之一为CH4(g)?C(s)+2H2(g),600℃之后,C的物质的量减少,请用方程式表示C减少的原因C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO.

(4)不同温度对CO2的转化率及催化剂的效率影响如图2所示,下列有关说法不正确的是①②④(填序号).
①不同条件下反应,N点的速率最大
②温度低于250℃时,随温度升高乙烯的产率增大
③M点时平衡常数比N点时平衡常数大
④实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)已知某温度下CO2(g)+CH4(g)?2CO(g)+2H2(g)的平衡常数为K1
H2O(g)+CH4(g)?CO(g)+3H2(g)的平衡常数为K2
C(s)+H2O(g)?2CO(g)+2H2(g)的平衡常数为K3
则反映C(g)+CO2(g)?2CO(g) 的平衡常数为K为$\frac{{K}_{3}{•K}_{1}}{{K}_{2}}$(用K1、K2、K3表示)
8.某有机物A用1H核磁共振分析得到如谱图,据此推测A的结构简式可能为( )

| A. | CH3CH2CH3 | B. | CH3CHO | C. | CH3CH2OH | D. | CH3CH2CH2COOH |
9.利用图1和图2中的信息,按图3装置(连接的A、B瓶中已充有NO2气体)进行实验.

下列说法正确的是( )

下列说法正确的是( )
| A. | H2O2中只含有极性共价键,不含离子键 | |
| B. | 2NO2?N2O4的平衡常数K随温度升高而减小 | |
| C. | 向H2O2中加入Fe2(SO4)3后,B中颜色变浅 | |
| D. | H2O2分解反应中Fe2(SO4)3作催化剂,可以使反应的△H减小 |
 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题: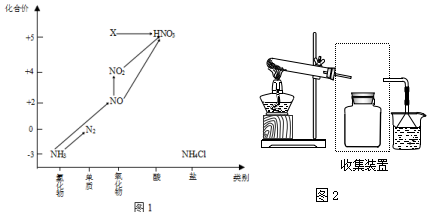

 Ⅰ.铁及铁的化合物应用广泛,如FeCl3可用作印刷电路铜版腐蚀剂和外伤止血剂等.
Ⅰ.铁及铁的化合物应用广泛,如FeCl3可用作印刷电路铜版腐蚀剂和外伤止血剂等.