题目内容
11.硫代硫酸钠与稀盐酸混合后缓慢发生反应:Na2S2O3+2HCl→2NaCl+S↓+SO2↑+H2O,现有两组实验①20℃时,向5.0mL0.20mol•L-1的盐酸中加入5.0mL0.36mol•L-1的Na2S2O3溶液
②20℃时,向5.0mL0.15mol•L-1的盐酸中加入2.5mL0.54mol•L-1的 Na2S2O3溶液,
则反应速率( )
| A. | ①>② | B. | ①=② | C. | ①<② | D. | 无法确定 |
分析 ①20℃时,向5.0mL0.20mol•L-1的盐酸中加入5.0mL0.36mol•L-1的Na2S2O3溶液,混合后盐酸的浓度为0.10mol•L-1,Na2S2O3的浓度为0.18mol•L-1,
②20℃时,向5.0mL0.15mol•L-1的盐酸中加入2.5mL0.54mol•L-1的 Na2S2O3溶液,混合后盐酸的浓度为0.10mol•L-1,Na2S2O3的浓度为0.18mol•L-1,
结合浓度对反应速率的影响解答该题.
解答 解:①20℃时,向5.0mL0.20mol•L-1的盐酸中加入5.0mL0.36mol•L-1的Na2S2O3溶液,混合后盐酸的浓度为$\frac{0.20×5}{5+5}$mol•L-1=0.10mol•L-1,Na2S2O3的浓度为$\frac{0.36×5}{5+5}$mol•L-1=0.18mol•L-1,
②20℃时,向5.0mL0.15mol•L-1的盐酸中加入2.5mL0.54mol•L-1的 Na2S2O3溶液,混合后盐酸的浓度为$\frac{0.15×5}{5+2.5}$mol•L-1=0.10mol•L-1,Na2S2O3的浓度为$\frac{2.5×0.54}{2.5+5}$mol•L-1=0.18mol•L-1,
两种溶液中浓度相同,则反应速率相同,
故选B.
点评 本题考查化学反应速率,为高考高频考点,侧重于反应速率的影响因素的考查以及数据处理能力,能较好的培养学生良好的科学素养,难度不大,学习中注意掌握影响化学反应速率的因素.

练习册系列答案
相关题目
1.制取氯乙烷(CH3-CH2Cl)的最好方法是( )
| A. | 乙烷与氯气发生取代反应 | B. | 乙烯与氯气发生加成反应 | ||
| C. | 乙烯与氯化氢发生加成反应 | D. | 甲烷与氯气发生取代反应 |
2.某款香水中的香氛主要由以下三种化合物构成,下列说法正确的是( )


| A. | 月桂烯分子中所有原子可能共平面 | |
| B. | 柠檬醛和香叶醇是同分异构体 | |
| C. | 香叶醇能发生加成反应、氧化反应、酯化反应 | |
| D. | 三种有机物的一氯代物均有7种(不考虑立体异构) |
6.下列做法中正确的是( )
| A. | 除去乙烷中少量的乙烯:与适量的氢气混合加热,把乙烯转化为乙烷 | |
| B. | 除去苯中的少量己烯:加入浓溴水振荡、静置后分液,除去己烯 | |
| C. | 验证丙烷中含有丙烯:通入溴水,溴水褪色 | |
| D. | 除去溴苯中的少量苯:加入水,振荡、静置分层后,取出上层即可分离 |
16.化合物是一种取代有机氯农药DDT的新型杀虫剂,它含有几种官能团( )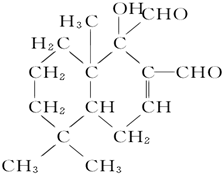

| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
3.分子式为C6H12,其中具有3个甲基的烯烃共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
 ,所含化学键类型为离子键、共价键.向甲中滴加足量水时发生反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
,所含化学键类型为离子键、共价键.向甲中滴加足量水时发生反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.