题目内容
6.下列做法中正确的是( )| A. | 除去乙烷中少量的乙烯:与适量的氢气混合加热,把乙烯转化为乙烷 | |
| B. | 除去苯中的少量己烯:加入浓溴水振荡、静置后分液,除去己烯 | |
| C. | 验证丙烷中含有丙烯:通入溴水,溴水褪色 | |
| D. | 除去溴苯中的少量苯:加入水,振荡、静置分层后,取出上层即可分离 |
分析 A.乙烯与氢气发生加成反应,乙烷中易引入新杂质氢气;
B.溴易溶于苯;
C.丙烯与溴水反应,而丙烷不能;
D.溴苯、溴均不溶于水.
解答 解:A.乙烯与氢气发生加成反应,乙烷中易引入新杂质氢气,不能除杂,应选溴水、洗气,故A错误;
B.溴易溶于苯,引入新杂质,可利用蒸馏法除去苯中的少量己烯,故B错误;
C.丙烯与溴水反应,而丙烷不能,则通入溴水,溴水褪色可验证,故C正确;
D.溴苯、溴均不溶于水,不能利用水除杂,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握有机物的性质、性质差异及混合物分离方法的选择为解答本题关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列有机物或有机物组合,在一定条件下不能发生聚合反应的是( )
| A. | 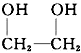 和HOOC-COOH 和HOOC-COOH | B. | HC≡CH | C. | 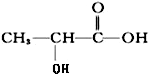 | D. | CH3COOH和C2H5OH |
17. 己烯雌酚是人工合成的非甾体雌激素物质,主要用于治疗雌激素低下症及激素平衡失调所引起的功能性出血等,如图所示分别取1 mol己烯雌酚进行4个实验.( )
己烯雌酚是人工合成的非甾体雌激素物质,主要用于治疗雌激素低下症及激素平衡失调所引起的功能性出血等,如图所示分别取1 mol己烯雌酚进行4个实验.( )
 己烯雌酚是人工合成的非甾体雌激素物质,主要用于治疗雌激素低下症及激素平衡失调所引起的功能性出血等,如图所示分别取1 mol己烯雌酚进行4个实验.( )
己烯雌酚是人工合成的非甾体雌激素物质,主要用于治疗雌激素低下症及激素平衡失调所引起的功能性出血等,如图所示分别取1 mol己烯雌酚进行4个实验.( )| A. | ①中生成7molH2O | B. | ②中无CO2生成 | ||
| C. | ③中最多消耗3molBr2 | D. | ④中发生消去反应 |
14.己烷雌酚的一种合成路线如下:
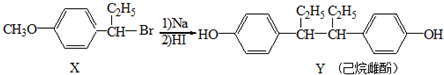
下列叙述正确的是( )

下列叙述正确的是( )
| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 在一定条件,化合物Y不能与HCHO发生缩聚反应 | |
| C. | 用FeCl3溶液可鉴别化合物X和Y | |
| D. | 1mol化合物Y可消耗3mol溴水发生取代反应 |
11.硫代硫酸钠与稀盐酸混合后缓慢发生反应:Na2S2O3+2HCl→2NaCl+S↓+SO2↑+H2O,现有两组实验
①20℃时,向5.0mL0.20mol•L-1的盐酸中加入5.0mL0.36mol•L-1的Na2S2O3溶液
②20℃时,向5.0mL0.15mol•L-1的盐酸中加入2.5mL0.54mol•L-1的 Na2S2O3溶液,
则反应速率( )
①20℃时,向5.0mL0.20mol•L-1的盐酸中加入5.0mL0.36mol•L-1的Na2S2O3溶液
②20℃时,向5.0mL0.15mol•L-1的盐酸中加入2.5mL0.54mol•L-1的 Na2S2O3溶液,
则反应速率( )
| A. | ①>② | B. | ①=② | C. | ①<② | D. | 无法确定 |
18.如表实验操作、现象和结论均正确的是选项实验操作现象结论( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 向稀硝酸溶液中加入过量铁粉充分反应后,滴加KSCN溶液 | 溶液变为血红色 | 稀硝酸具有氧化性,能将Fe氧化成Fe3+ |
| C | KNO3和KOH混合溶液中加入铝粉 并加热,管口放湿润的红色石蕊试纸 | 试纸变为蓝色 | NO3-还原为NH3 |
| D | 向两份蛋白质溶液中分别滴加 Na2SO4溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| A. | A | B. | B | C. | C | D. | D |
15.除去SiO2中混有的少量生石灰和石灰石,有如下操作:( )
①加水溶解 ②加水煮沸 ③过滤 ④加稀HCl.
①加水溶解 ②加水煮沸 ③过滤 ④加稀HCl.
| A. | ①③ | B. | ④③ | C. | ⑤③ | D. | ②③ |
16. 氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,按要求完成下列问题:
氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,按要求完成下列问题:
(1)该滴定实验应选用酸(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液,原因是高锰酸钾溶液具有强氧化性能氧化橡胶管.
(2)写出酸性高锰酸钾与草酸反应的离子方程式2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.
(3)滴定终点的现象为滴入最后一滴高锰酸钾,锥形瓶中的溶液恰好从无色变为浅紫色,且30s内不变色.
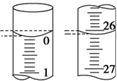
(4)甲同学在滴定开始和结束时,观察到装标准液的滴定管的液面如图所示,则本次滴定所消耗标准液的体积为26.10mL.
(5)乙学生按照滴定步骤进行了3次实验,分别记录有关数据如表:
依据上表数据计算该H2C2O4溶液的物质的量浓度为0.2610mol/L(保留4位有效数字).
(6)下列操作中可能使测定结果偏低的是CD(填字母).
A.酸式滴定管未用标准液润洗就直接注入KMnO4标准液
B.滴定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴部分在滴定前没有气泡,滴定后有气泡
D.读取KMnO4标准液时,开始仰视读数,滴定结束时俯视读数
(7)草酸是二元弱酸,草酸氢钾在水中电离程度大于水解程度.向10mL0.01mol/L的H2C2O4溶液中滴加0.01mol/LKOH溶液V(mL),当V=a mL时,溶液中满足c(C2O42-)+c(OH-)=c(H+)+c(H2C2O4),则a的数值为10,此时溶液呈酸(填“酸性”或“碱性”或“中性”).
 氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,按要求完成下列问题:
氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,按要求完成下列问题:(1)该滴定实验应选用酸(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液,原因是高锰酸钾溶液具有强氧化性能氧化橡胶管.
(2)写出酸性高锰酸钾与草酸反应的离子方程式2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.
(3)滴定终点的现象为滴入最后一滴高锰酸钾,锥形瓶中的溶液恰好从无色变为浅紫色,且30s内不变色.
(4)甲同学在滴定开始和结束时,观察到装标准液的滴定管的液面如图所示,则本次滴定所消耗标准液的体积为26.10mL.
(5)乙学生按照滴定步骤进行了3次实验,分别记录有关数据如表:
| 滴定次数 | 待测H2C2O4溶液的体积/mL | 0.1000mol•L-1 KMnO4的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(6)下列操作中可能使测定结果偏低的是CD(填字母).
A.酸式滴定管未用标准液润洗就直接注入KMnO4标准液
B.滴定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴部分在滴定前没有气泡,滴定后有气泡
D.读取KMnO4标准液时,开始仰视读数,滴定结束时俯视读数
(7)草酸是二元弱酸,草酸氢钾在水中电离程度大于水解程度.向10mL0.01mol/L的H2C2O4溶液中滴加0.01mol/LKOH溶液V(mL),当V=a mL时,溶液中满足c(C2O42-)+c(OH-)=c(H+)+c(H2C2O4),则a的数值为10,此时溶液呈酸(填“酸性”或“碱性”或“中性”).
 ;
;