题目内容
下列关于热化学反应的描述中正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B、碳与二氧化碳的反应既是吸热反应,又是化合反应 |
| C、热化学方程式中化学计量数可表示分子个数 |
| D、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
考点:热化学方程式
专题:化学反应中的能量变化
分析:A、中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量;
B、C与CO2的反应是以碳为还原剂的氧化还原反应,是吸热反应;
C、反应热△H的单位是KJ/mol;
D、燃烧热是指25℃101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.
B、C与CO2的反应是以碳为还原剂的氧化还原反应,是吸热反应;
C、反应热△H的单位是KJ/mol;
D、燃烧热是指25℃101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.
解答:
解:A、中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量,其衡量标准是生成的水为1mol,故无论稀H2SO4和Ca(OH)2反应生成的水是几摩尔,其中和热恒为57.3KJ/mol,故A错误;
B、C与CO2的反应是以碳为还原剂的氧化还原反应:C+CO2=2CO,是吸热反应也是化合反应,故B正确;
C、反应热△H的单位是KJ/mol,故热化学方程式中化学计量数只能代表物质的量,故C错误;
D、燃烧热是指在25℃101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,此时生成的水必须为液态,故D错误.
故选B.
B、C与CO2的反应是以碳为还原剂的氧化还原反应:C+CO2=2CO,是吸热反应也是化合反应,故B正确;
C、反应热△H的单位是KJ/mol,故热化学方程式中化学计量数只能代表物质的量,故C错误;
D、燃烧热是指在25℃101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,此时生成的水必须为液态,故D错误.
故选B.
点评:本题考查了燃烧热、中和热以及热化学方程式中计量数的含义,难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
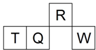 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与主族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与主族序数相等.下列判断不正确的是( )| A、R元素的最简单气态氢化物极易溶于水 |
| B、最高价氧化物对应水化物的酸性:W>Q |
| C、原子半径:T>R |
| D、含T元素的盐溶液一定显碱性 |
酸雨是指pH<5.6的雨水.你认为减少酸雨产生的途径可采取的措施是:( )
①用煤作燃料,②把工厂烟囱造高,③燃料脱硫处理,④开发新能源,⑤在已酸化的土壤中加石灰.
①用煤作燃料,②把工厂烟囱造高,③燃料脱硫处理,④开发新能源,⑤在已酸化的土壤中加石灰.
| A、①②③ | B、②③④⑤ |
| C、③④ | D、③④⑤ |
通常状况下,NC13是一种油状液体,其分子空间构型与氨分子相似,下列对NC13的有关叙述正确的是( )
| A、分子中N-C1键键长比CCl4分子中C-C1键键长长 |
| B、分子中的所有原于均达到8电子稳定结构 |
| C、NCl3分子是非极性分子 |
| D、NBr3比NCl3易挥发 |
把70%的硝酸溶液(ρ=1.40g/cm3)加到等体积的水中,则稀释后硝酸溶液中溶质的质量分数为( )
| A、等于35% | B、小于35% |
| C、大于35% | D、无法确定 |
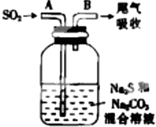 硫、氯及其化合物由广泛的用途.
硫、氯及其化合物由广泛的用途.