题目内容
19.某有机物的结构简式为 ,关于它的叙述中正确的是( )
,关于它的叙述中正确的是( )| A. | 1mol该有机物最多能够和2molNaOH发生反应 | |
| B. | 和乙醇发生酯化反应时,羧基中的-OH将被CH3CH2-取代 | |
| C. | 铜做催化剂并加热的条件下,羟基中的氢氧键会断裂 | |
| D. | 和  互为同分异构体 互为同分异构体 |
分析 有机物含有碳碳双键,可发生加成、加聚和氧化反应,含有羟基,可发生取代、氧化和消去反应,含有羧基,具有酸性,可发生中和、酯化反应,以此解答该题.
解答 解:A.只有羧基与氢氧化钠反应,则1mol该有机物最多能够和1molNaOH发生反应,故A错误;
B.和乙醇发生酯化反应时,羧基断裂C-O键,乙醇断裂O-H键,羧基中的-OH将被CH3CH2O-取代,故B错误;
C.含有羟基,可发生催化氧化,则铜做催化剂并加热的条件下,羟基中的氢氧键会断裂,故C正确;
D.和  分子式不同,不是同分异构体,故D错误.
分子式不同,不是同分异构体,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答本题关键,侧重分析与应用能力的考查,注意烯烃、羧酸性质的应用,题目难度不大.

练习册系列答案
相关题目
9.如表是元素周期表的一部分,回答下列问题:
(1)在这些元素中,F(用元素符号填写,下同)是最活泼的非金属元素;Ar是最不活泼的元素.
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;能形成两性氢氧化物的元素是Al.
(3)从⑤到⑪的元素中,Cl原子半径最小,写出③形成的氢化物的结构式H-O-H.
(4)比较⑤与⑥的化学性质,Na更活泼,试用实验证明(简述简单操作、主要现象和结论把钠镁分别投入冷水中,钠不断游动,不一会儿就消失,而镁无明显现象,故可知钠比镁活泼.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;能形成两性氢氧化物的元素是Al.
(3)从⑤到⑪的元素中,Cl原子半径最小,写出③形成的氢化物的结构式H-O-H.
(4)比较⑤与⑥的化学性质,Na更活泼,试用实验证明(简述简单操作、主要现象和结论把钠镁分别投入冷水中,钠不断游动,不一会儿就消失,而镁无明显现象,故可知钠比镁活泼.
10.聚氯乙烯简称PVC,是当今世界上产量最大、应用最广的热塑性塑料之一.下列说法正确的是( )
| A. | 聚氯乙烯的单体是CH3CH2Cl | |
| B. | 聚氯乙烯是高分子化合物 | |
| C. | 聚氯乙烯能够使溴的四氯化碳溶液褪色 | |
| D. | 聚氯乙烯保鲜膜最适合用来包装蔬菜、水果及熟食 |
11.下列物质中没有酸性的是( )
| A. | Al2O3 | B. | H2SO4 | C. | KClO3 | D. | NaHSO4 |
8.下列关于二氧化硅的叙述正确的是( )
| A. | SiO2的用途广泛,主要用途是用于做半导体材料 | |
| B. | SiO2不与任何酸或碱性性氧化物反应 | |
| C. | SiO2和CO2的结构不同,但它们都具有氧化性,都能与强碱反应 | |
| D. | 因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 |
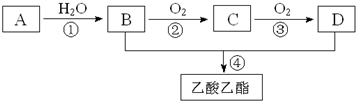
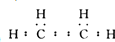 ,其空间构型平面形.
,其空间构型平面形.