题目内容
3.已知S和Cl两种元素均位于第三周期,则( )| A. | 原子半径:S<Cl | |
| B. | 元素非金属性:S>Cl | |
| C. | 氢化物的稳定性:H2S>HCl | |
| D. | 最高价氧化物对应水化物的酸性:H2SO4<HClO4 |
分析 A.同一周期中,原子序数越大原子半径越小;
B.同一周期中原子序数越大,非金属性越弱;
C.非金属性越强,对应简单氢化物的稳定性越强;
D.非金属性越强,最高价含氧酸的酸性越强.
解答 解:A.S、Cl位于第三周期,原子序数S<Cl,则原子半径S>Cl,故A错误;
B.S、Cl位于第三周期,同一周期中原子序数越大非金属性越强,原子序数S<Cl,则元素非金属性:S<Cl,故B错误;
C.元素非金属性:S<Cl,则简单氢化物的稳定性:H2S<HCl,故C错误;
D.元素非金属性:S<Cl,最高价氧化物对应水化物的酸性:H2SO4<HClO4,故D正确;
故选D.
点评 本题考查原子结构与元素周期律的关系,题目难度不大,明确元素周期律的内容为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题有利于提高学生的综合应用能力.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
13.NO2被水吸收发生反应:3NO2+H2O=2HNO3+NO,该反应中发生还原反应的物质和发生氧化反应的物质的质量比为( )
| A. | 1:2 | B. | 2:1 | C. | 1:3 | D. | 3:1 |
14.某学习小组探究温度对Fe3+水解的影响.通过测量不同温度下溶液透光率(对光的透过能力)的变化判断平衡移动的方向.一般情况下溶液颜色越深,透光率越小.
(1)Fe3+(aq)+3H2O(l)?Fe(OH)3(aq)+3H+(aq)△H>0
①加热,溶液颜色变深,平衡向右移动.
②通常在FeCl3溶液中加入少量HCl,目的是抑制铁离子水解.
(2)探究温度对Fe3+水解的影响.
【假设】当温度升高时,Fe3+水解平衡正向移动,溶液的颜色会变深,透光率减小;如果降温时反应可逆回,则溶液的颜色应该变浅,透光率增大.
【实验】分别加热0.5mol/LFe(NO3)3、FeCl3溶液(均未酸化)至50℃后停止加热,自然冷却.测得的温度变化曲线及透光率变化曲线如图所示.
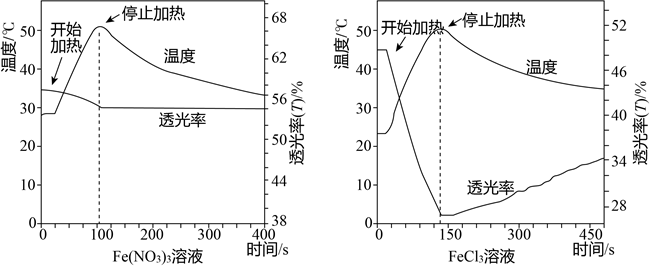
①Fe(NO3)3、FeCl3溶液浓度相同,目的是保证铁离子浓度相等.
②小组依据变化曲线推测:FeCl3溶液颜色随温度变化的改变可能不完全是由水解平衡引起的.推测的根据是0.5mol/LFe(NO3)3、FeCl3溶液(均未酸化),50℃后停止加热,自然冷却,两者透光率不同.
(3)为证实小组推测,实验如下:
①实验a、b加入大量HNO3的作用是抑制水解,这样做的目的是为验证阴离子不同对铁离子水解的影响.
②小组推测是否合理,说明理由合理,阴离子不同,溶液颜色不同.
(4)【查阅文献】Fe3++nCl-?[FeCln]3-n(黄色)△H>0(n=1~4).该平衡可以解释FeCl3溶液实验的现象,通过如下实验得到了证实.
【实验】(将实验过程补充完整):
结果与讨论:加热能促进Fe3+的水解,但降温时逆回程度较小;溶液颜色与阴离子有关.
(1)Fe3+(aq)+3H2O(l)?Fe(OH)3(aq)+3H+(aq)△H>0
①加热,溶液颜色变深,平衡向右移动.
②通常在FeCl3溶液中加入少量HCl,目的是抑制铁离子水解.
(2)探究温度对Fe3+水解的影响.
【假设】当温度升高时,Fe3+水解平衡正向移动,溶液的颜色会变深,透光率减小;如果降温时反应可逆回,则溶液的颜色应该变浅,透光率增大.
【实验】分别加热0.5mol/LFe(NO3)3、FeCl3溶液(均未酸化)至50℃后停止加热,自然冷却.测得的温度变化曲线及透光率变化曲线如图所示.

①Fe(NO3)3、FeCl3溶液浓度相同,目的是保证铁离子浓度相等.
②小组依据变化曲线推测:FeCl3溶液颜色随温度变化的改变可能不完全是由水解平衡引起的.推测的根据是0.5mol/LFe(NO3)3、FeCl3溶液(均未酸化),50℃后停止加热,自然冷却,两者透光率不同.
(3)为证实小组推测,实验如下:
| 编号 | 实验 | 操作及现象 |
| a | 向Fe(NO3)3溶液(棕黄色)中加入大量HNO3 | i.溶液颜色非常浅 ii.加热和降温过程中透光率无明显变化 |
| b | 向FeCl3溶液(黄色)中加入大量HNO3 | i.溶液仍为黄色 ii.加热透光率下降,降温透光率上升 |
②小组推测是否合理,说明理由合理,阴离子不同,溶液颜色不同.
(4)【查阅文献】Fe3++nCl-?[FeCln]3-n(黄色)△H>0(n=1~4).该平衡可以解释FeCl3溶液实验的现象,通过如下实验得到了证实.
【实验】(将实验过程补充完整):
| 编号 | 实验 | 操作及现象 |
| c | 向Fe(NO3)3溶液中加入大量HNO3,再加入几滴NaCl溶液. | 测此溶液透光率随温度改变的变化情况,增加氯离子浓度,有色离子浓度增加 |
8.下列实验操作、实验现象及所得出的结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Na2SiO3溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色退去 | 2min后,出现凝胶 | 酸性:HCl>H2SiO3 |
| B | 在SiO2中加入蒸馏水,振荡 | SiO2溶解 | SiO2是H2SiO3的酸酐 |
| C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁与浓硫酸不反应 |
| D | 向某溶液中先滴加少量氯水,一会儿后滴加KSCN溶液 | 滴加氯水时无明显现象,滴加KSCN溶液后,混合液变成红色 | 原溶液中含有Fe2+,没有Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
15.常温下,在pH=1的某溶液中可能有Na+、Fe3+、Fe2+、I-、Cl-、CO32-中的几种,现取100mL该溶液进行如下实验.根据实验结果,下列判断正确的是( )

| A. | Fe3+、I-、Cl-三种离子一定存在 | |
| B. | CO32-一定不存在,不能确定Na+和Cl-是否存在 | |
| C. | Fe3+与Fe2+至少有一种 | |
| D. | 该溶液中c(Cl-)至少为0.2mol•L?1 |
12.下列物质中,含极性共价键的化合物是( )
| A. | NaCl | B. | Cl2 | C. | HCl | D. | H2 |
13.下列关于乙烯和苯的叙述中,错误的是( )
| A. | 乙烯能发生加聚反应 | B. | 乙烯可以燃烧 | ||
| C. | 苯能使酸性高锰酸钾溶液褪色 | D. | 苯分子中6个碳碳化学键完全相同 |