题目内容
11.下列烷烃的命名正确的是( )| A. | 2-甲基丁烷 | B. | 2-乙基丁烷 | ||
| C. | 3-甲基丁烷 | D. | 1,3,3-三甲基丙烷 |
分析 A.丁烷说明最长碳链为4个碳原子,可以存在2-甲基;
B.烷烃的命名中不能存在2-乙基;
C.离支链最近一端编号;
D.烷烃命名中1号碳原子上不能连接烷基.
解答 解:A.丁烷说明最长碳链为4个碳原子,可以存在2-甲基,2-甲基丁烷符合烷烃的系统命名规则,故A正确;
B.2-乙基丁烷,不符合主碳链最长,不存在2-乙基,故B错误;
C.离支链最近一端编号,应为2-甲基丁烷,故C错误;
D.1,1,3-三甲基戊烷,不符合碳链最长,烷烃中无1-甲基存在,故D错误;
故选A.
点评 本题考查了烷烃的命名,题目难度不大,该题的关键是明确有机物的命名原则,然后结合有机物的结构特点灵活运用即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.苯佐卡因(对氨基苯甲酸乙酯)为白色粉末,常用于创面、溃疡面及痔疮的镇痛.实验室制备苯佐卡因的反应、装置示意图和有关数据如下:
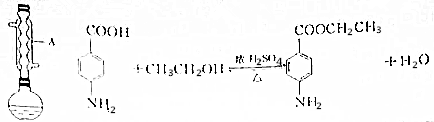
实验步骤:在圆底烧瓶中加入2~3片碎瓷片,0.00300mol对氨基苯甲酸、0.0150mol乙醇和数滴浓硫酸,振荡,然后将烧瓶在水浴上加热回流1h,冷却后,分批加入NaHCO3溶液直至无明显气泡产生,再加入少量NaHCO3溶液至pH≈8.将烧瓶中的液体倒入分液漏斗中,用乙醚分两次萃取,向分液所得的乙醚层中加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,最后蒸馏,蒸出乙醚,得苯佐卡因0.198g.
回答下列问题:
(1)仪器A的名称是球形冷凝管.
(2)碎瓷片的作用是防止暴沸.
(3)本实验中加入过量乙醇的目的是提高对氨基苯甲酸的利用率.
(4)加入NaHCO3溶液的作用是除去混有对氨基苯甲酸.
(5)分液漏斗使用之前必须进行的操作是查漏;分液时,应先将下层液从分液漏斗下口放出,再将上层液从上口倒出.
(6)实验中加入少量无水硫酸镁的目的是吸收乙醚中的水.
(7)本实验中苯佐卡因的产率是40%(保留三位有效数字).
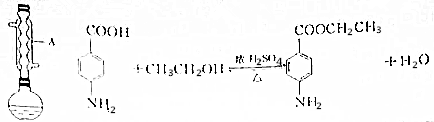
| 相对分子质量 | 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | 水中溶解性 | |
| 乙醇 | 46 | 0.789 | -117.3 | 78.5 | 与水互溶 |
| 对氨基苯甲酸 | 137 | 1.374 | 188 | 340 | 微溶 |
| 苯佐卡因 | 165 | 1.039 | 90 | 172 | 难溶 |
| 乙醚 | 74 | 0.71 | -116.3 | 35 | 微溶 |
回答下列问题:
(1)仪器A的名称是球形冷凝管.
(2)碎瓷片的作用是防止暴沸.
(3)本实验中加入过量乙醇的目的是提高对氨基苯甲酸的利用率.
(4)加入NaHCO3溶液的作用是除去混有对氨基苯甲酸.
(5)分液漏斗使用之前必须进行的操作是查漏;分液时,应先将下层液从分液漏斗下口放出,再将上层液从上口倒出.
(6)实验中加入少量无水硫酸镁的目的是吸收乙醚中的水.
(7)本实验中苯佐卡因的产率是40%(保留三位有效数字).
2.25℃时,Ksp(AgC1)=1.8×10-10,Ksp(AgI)=8.5×10-17,则下列说法正确的是( )
| A. | 向饱和AgCl水溶液中加入盐酸,Ksp(AgC1)变大 | |
| B. | AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) | |
| C. | 温度一定,当溶液中c(Ag+)c(Cl- )<Ksp(AgCl)时,此溶液中必有AgCl沉淀析出 | |
| D. | 向AgI的悬浊液中加NaCl浓溶液,可能有AgCl生成 |
6.S2Cl2是工业上常用的硫化剂,是一种金黄色液体.
已知:①S2Cl2不稳定,进一步氧化可得SCl2
②S2Cl2和SCl2 都与水反应,2S2Cl2+2H2O═3S↓+SO2↑+4HCl,3SCl2+4H2O═2S↓+H2SO4+64HCl
③几种物质的熔沸点如表:
如图是实验室中通过向熔融的单质硫中通入少量Cl2制取S2Cl2的装置(部分夹持、加热装置已略去)
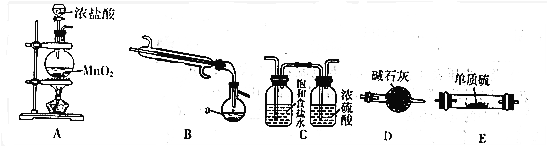
(1)B装置中仪器a的名称蒸馏烧瓶.
(2)装置的连接顺序是(每个装置只能使用一次)ACEBD.
(3)装置D的作用是防止空气中的水蒸气进入装置B,吸收多余的氯气.
(4)实验中先点燃A装置酒精灯制取Cl2时,当当E中充满黄绿色的气体时,说明排净空气,再点燃E处酒精灯.
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是蒸馏,该操作的温度范围是59℃~137℃.
(6)请设计实验验证所得产品中是否含有杂质SCl2:取少量产品加入试管中,再加入适量蒸馏水,振荡、静置.取少量上层清夜,滴加氯化钡溶液,若有白色沉淀生成,证明有S2Cl2,否则无S2Cl2.
已知:①S2Cl2不稳定,进一步氧化可得SCl2
②S2Cl2和SCl2 都与水反应,2S2Cl2+2H2O═3S↓+SO2↑+4HCl,3SCl2+4H2O═2S↓+H2SO4+64HCl
③几种物质的熔沸点如表:
| 物质 | S | SCl2 | S2Cl2 |
| 沸点/℃ | 445 | 59 | 137 |
| 熔点/℃ | 113 | -122 | -77 |

(1)B装置中仪器a的名称蒸馏烧瓶.
(2)装置的连接顺序是(每个装置只能使用一次)ACEBD.
(3)装置D的作用是防止空气中的水蒸气进入装置B,吸收多余的氯气.
(4)实验中先点燃A装置酒精灯制取Cl2时,当当E中充满黄绿色的气体时,说明排净空气,再点燃E处酒精灯.
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是蒸馏,该操作的温度范围是59℃~137℃.
(6)请设计实验验证所得产品中是否含有杂质SCl2:取少量产品加入试管中,再加入适量蒸馏水,振荡、静置.取少量上层清夜,滴加氯化钡溶液,若有白色沉淀生成,证明有S2Cl2,否则无S2Cl2.
16.常温下,下列溶液的离子浓度关系式正确的是( )
| A. | 浓度相同的Na2CO3和NaHCO3混合溶液中,c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) | |
| B. | 0.1mol/L①醋酸②氯化铵③硫酸溶液中,水电离产生的氢离子浓度大小顺序是②>①>③ | |
| C. | 0.1mol/L的NaHCO3溶液中 C(Na+)+c(H+)=c(OH-)+c(HCO3-) | |
| D. | pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):③>②>① |
3.短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍,也是C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和.下列说法正确的是( )
| A. | 原子半径C>D>E,三者形成的简单离子中D离子的半径最小 | |
| B. | 元素A所形成的氢化物常温下一定为气态 | |
| C. | 元素C、D、E在自然界中均不能以游离态存在 | |
| D. | 元素B的氧化物对应的水化物一定为强酸 |
1.如图实验现象预测正确的是( )
| A. | 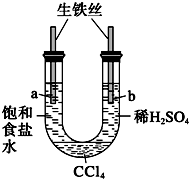 一段时间后,a管液面高于b管液面并且a处溶液的pH增大,b处溶液的pH 减小 | |
| B. |  继续煮沸溶液至红褐色,停止加热,当光束通过体系时无丁达尔效应 | |
| C. | 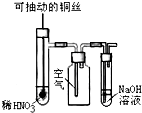 微热稀HNO3溶液片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 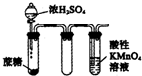 酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |