题目内容
15.原子序数依次增大的四种短周期元素X,Y,Z,M.其中Z是金属元素,X的原子半径小于Y,Y与M同主族,Y的质子数为M的$\frac{1}{2}$,下列说法一定正确的是( )| A. | X与M的原子序数之差为31 | |
| B. | Y的离子半径小于Z的离子半径 | |
| C. | 由X与Z组成的化合物,可与水反应放出X2 | |
| D. | 由M与Y组成的化合物,其水化物是强酸 |
分析 Y与M同主族,Y的质子数为M的$\frac{1}{2}$,则Y为O元素,M为S元素,X的原子半径小于Y,且原子序数小于Y,则X应位于Y的上一周期,应为第一周期元素,Z为金属,可能为Na、Mg、Al等,以此解答该题.
解答 解:Y与M同主族,Y的质子数为M的$\frac{1}{2}$,则Y为O元素,M为S元素,X的原子半径小于Y,且原子序数小于Y,则X应位于Y的上一周期,应为第一周期元素,Z为金属,可能为Na、Mg、Al等,
A.M为S元素,原子序数为16,则与X的原子序数不肯能为31,故A错误;
B.Y为O元素,Z为金属,可能为Na、Mg、Al等,对应的离子具有相同的核外电子排布,核电荷数越大,离子半径越小,故B错误;
C.如X为H,与金属形成的氢化物可与水反应生成氢气,故C正确;
D.如生成二氧化硫,对应的亚硫酸为弱酸,故D错误.
故选C.
点评 本题考查原子结构和性质,侧重考查分析、推断能力,涉及元素周期律、原子结构、物质结构、化学键等知识点,注意把握原子的结构特点,难度不大.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
20.设阿伏加德罗常数的值为NA,则下列说法不正确的是( )
| A. | 1mol Na参加氧化还原反应时电子转移NA | |
| B. | 3.2g SO2与2.3g NO2所含有的氧原子数相等 | |
| C. | 标准状况下,2.24L H2O含有的O原子数为0.1NA | |
| D. | 1L 0.1mol/LMgCl2溶液中Cl-离子数为0.2NA |
6. 乙酸正丁酯是一种重要化工原料,某实验小组利用图1、图2装置合成乙酸正丁酯(夹持装置已略去),发生的化学反应为:
乙酸正丁酯是一种重要化工原料,某实验小组利用图1、图2装置合成乙酸正丁酯(夹持装置已略去),发生的化学反应为:
CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
可能用到的有关数据见下表:
实验步骤如下:
①在圈1的圆底烧瓶中,装入7.Og正丁醇和7.Og冰醋酸,再加入3-4滴浓硫酸.
②如图1所示,安装分水器和回流冷凝管.加热圆底烧瓶,待反应基本完成后,停止加誊
③冷却后将分水器中分出的酯层和圆底烧瓶中的反应液一起倒入分液漏斗中.先后用水、10%碳酸钠溶液洗涤.分离得到的酯层再用水洗涤后倒入锥形瓶中,加无水硫酸镁干燥.
④将干燥后的酯层倒入图2的蒸馏烧瓶中,加热蒸馏.收集124℃-126℃的馏分,称得质量为7.0g.
回答下列问题:
(1)图2冷凝管中冷水从b口流入(用字母表示);仪器d的名称是尾接管.
(2)分液漏斗使用前须检漏并洗净备用.分离上下层液体时,应先打开分液漏斗上端的玻璃塞,然后打开活塞放出下层液体,上层液体从上口倒出.
(3)实验中产生的副产物的结构简式为CH3CH2CH=CH2(任写一种).用10%碳酸钠溶液洗涤的主要目的是除去产品中含有的乙酸、硫酸等杂质.
(4)实验中国1圆底烧瓶c的容积最适合的是B(选填字母).
A.25mL B.50mL C.250mL D.500mL
(5)分水器中预先加水至略低于支管口.在加热过程中,除去生成水的操作是打开分水器下端的活塞,让水流出:判断
反应基本完成的标志是分水器中水面高度基本不再变化.
(6)实验中,乙酸正丁酯的产率为63.8%.
 乙酸正丁酯是一种重要化工原料,某实验小组利用图1、图2装置合成乙酸正丁酯(夹持装置已略去),发生的化学反应为:
乙酸正丁酯是一种重要化工原料,某实验小组利用图1、图2装置合成乙酸正丁酯(夹持装置已略去),发生的化学反应为:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
可能用到的有关数据见下表:
| 相对分子质量 | 沸点/℃ | 密度(g/cm3) | 水中溶解度 | |
| 正丁醇 | 74 | 117.2 | 0.80 | 微溶 |
| 乙酸 | 60 | 118.1 | 1.05 | 易溶 |
| 乙酸正丁酯 | 116 | 126.5 | 0.90 | 微溶 |
①在圈1的圆底烧瓶中,装入7.Og正丁醇和7.Og冰醋酸,再加入3-4滴浓硫酸.
②如图1所示,安装分水器和回流冷凝管.加热圆底烧瓶,待反应基本完成后,停止加誊
③冷却后将分水器中分出的酯层和圆底烧瓶中的反应液一起倒入分液漏斗中.先后用水、10%碳酸钠溶液洗涤.分离得到的酯层再用水洗涤后倒入锥形瓶中,加无水硫酸镁干燥.
④将干燥后的酯层倒入图2的蒸馏烧瓶中,加热蒸馏.收集124℃-126℃的馏分,称得质量为7.0g.
回答下列问题:
(1)图2冷凝管中冷水从b口流入(用字母表示);仪器d的名称是尾接管.
(2)分液漏斗使用前须检漏并洗净备用.分离上下层液体时,应先打开分液漏斗上端的玻璃塞,然后打开活塞放出下层液体,上层液体从上口倒出.
(3)实验中产生的副产物的结构简式为CH3CH2CH=CH2(任写一种).用10%碳酸钠溶液洗涤的主要目的是除去产品中含有的乙酸、硫酸等杂质.
(4)实验中国1圆底烧瓶c的容积最适合的是B(选填字母).
A.25mL B.50mL C.250mL D.500mL
(5)分水器中预先加水至略低于支管口.在加热过程中,除去生成水的操作是打开分水器下端的活塞,让水流出:判断
反应基本完成的标志是分水器中水面高度基本不再变化.
(6)实验中,乙酸正丁酯的产率为63.8%.
10.下列离子方程式正确的是( )
| A. | SO2通入Ca(ClO)2溶液中:SO2+Ca(ClO)2+H2O═CaSO3↓+2HClO | |
| B. | 常温下Fe和浓HNO3:Fe+6H++3NO3ˉ═Fe3++3NO2↑+3H2O | |
| C. | 向Fe(NO3)2溶液中加入稀 H2SO4:3Fe2++NO3ˉ+4H+═3Fe3++NO↑+2H2O | |
| D. | F2通入NaCl溶液中:F2+2Clˉ═2Fˉ+Cl2 |
20.25℃,有c(CH3COOH)+c(CH3COO-)═0.1mol•L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示.下列叙述不正确的是( )

| A. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 由图可知该温度下醋酸的电离常数为1×10-4.75 | |
| C. | pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol•L-1 | |
| D. | 向1L W点所表示溶液中通入0.05molHCl气体(溶液体积变化可忽略):2c(H+)+c(CH3COOH)═c(CH3COO-)+2c(OH-)+2 c(Cl-) |
7.有下列三个反应:①Cl2+FeI2═FeCl2+I2 ②2Fe2++Br2═2Fe3++2Br- ③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O下列说法正确的是( )
| A. | ①②③中的氧化产物分别是I2、Fe3+、CoCl2 | |
| B. | 根据以上方程式可以得到氧化性Cl2>Fe3+>Co2O3 | |
| C. | 在③反应中当1molCo2O3参加反应时,2molHCl被氧化 | |
| D. | 可以推理得到Cl2+FeBr2═FeCl2+Br2 |
 苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效.苹果醋是一种常见的有机酸,其结构简式如图所示.
苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效.苹果醋是一种常见的有机酸,其结构简式如图所示.
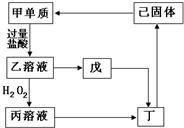 已知甲、乙、丙、丁、戊、己六种物质中含同一种元素,它们之间的转化关系如图所示.其中,丁是一种红褐色沉淀,戊是一种白色沉淀.请回答下列问题:
已知甲、乙、丙、丁、戊、己六种物质中含同一种元素,它们之间的转化关系如图所示.其中,丁是一种红褐色沉淀,戊是一种白色沉淀.请回答下列问题: