题目内容
在等物质的量浓度的![]() 溶液中,分别通入适量的
溶液中,分别通入适量的![]() 发生如下反应:
发生如下反应:
![]()
![]()
现有等物质的量浓度的![]() 4种溶液,其pH的关系为
4种溶液,其pH的关系为
[ ]
A.![]()
B.![]()
C.![]()
D.![]()
解析:
|
由反应 |

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案下列说法正确的是( )
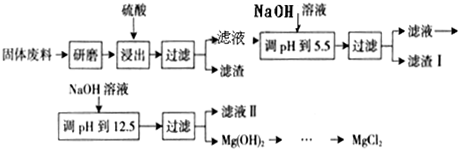
A.用坩埚灼烧MgCl2·6H2O的反应式 MgCl2·6H2OMgCl2+6H2O
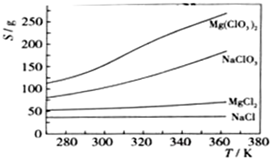
B.根据下表提供的数据,等物质的量浓度的NaClO、NaHCO3混合溶液中,有c(HCO3-)>c(ClO-)>c(OH-) 。
| 化学式 | 电离常数 |
| HClO | K1=3×10-8 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
C.常温下,将pH=2的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一。
D.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,溶度积常数Ksp=c(Ba2+)·c(SO42-)。则加入 Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d 点变到c 点。
阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
阴离子 | OH-、Cl-、 |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为:____________。
(2)写出E溶液与过量的B溶液反应的离子方程式:__________________________。
(3)已知:NaOH(aq)+HNO3(aq)![]() NaNO3(aq)+H2O(l);ΔH=-akJ·mol-1。请写出B与C的稀溶液反应的热化学方程式:____________________________________________________。
NaNO3(aq)+H2O(l);ΔH=-akJ·mol-1。请写出B与C的稀溶液反应的热化学方程式:____________________________________________________。
(4)在100 mL0.1 mol·L-1E溶液中,逐滴加入35mL2mol·L-1 NaOH溶液,最终得到沉淀的物质的量为__________________。