题目内容
 A、B、C、D、E、F为原子序数依次增大的前20号元素,已知A有多种核素,其中一种没有中子,B和C,C和E分别相邻,D的次外层电子数是最外层电子数的两倍.B、E、F的最外层电子数之和为12.
A、B、C、D、E、F为原子序数依次增大的前20号元素,已知A有多种核素,其中一种没有中子,B和C,C和E分别相邻,D的次外层电子数是最外层电子数的两倍.B、E、F的最外层电子数之和为12.(1)D、C形成的化合物在通讯上的重要用途
(2)E与F两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)用化学方程式表示B、D两种元素的非金属性强弱
(4)写出C、F两元素形成原子个数比为1:1的化合物甲的电子式
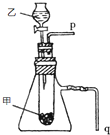
(5)甲可与一种常温下呈液态的常见化合物乙反应,若用如图装置来证明此反应①是放热反应,②生成了C的单质.简单合理的实验操作是:①
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E、F为原子序数依次增大的前20号元素,A有多种核素,其中一种没有中子,则A是H元素;
D的次外层电子数是最外层电子数的两倍,D元素前有多种元素,所以D的次外层为L层,则D最外层电子式是4,则D是Si元素;
B和C、C和E分别相邻,且这几种元素都是短周期元素,E为第三周期元素,所以B和C位于第二周期,E最外层电子数大于4而小于8,B的最外层电子数比E少1,B、E、F的最外层电子数之和为12,且这几种元素原子序数小于20,则符合条件的只有B是N、C是O、E是S、F是K元素,
再结合物质的结构和性质解答.
D的次外层电子数是最外层电子数的两倍,D元素前有多种元素,所以D的次外层为L层,则D最外层电子式是4,则D是Si元素;
B和C、C和E分别相邻,且这几种元素都是短周期元素,E为第三周期元素,所以B和C位于第二周期,E最外层电子数大于4而小于8,B的最外层电子数比E少1,B、E、F的最外层电子数之和为12,且这几种元素原子序数小于20,则符合条件的只有B是N、C是O、E是S、F是K元素,
再结合物质的结构和性质解答.
解答:
解:A、B、C、D、E、F为原子序数依次增大的前20号元素,A有多种核素,其中一种没有中子,则A是H元素;
D的次外层电子数是最外层电子数的两倍,D元素前有多种元素,所以D的次外层为L层,则D最外层电子式是4,则D是Si元素;
B和C、C和E分别相邻,且这几种元素都是短周期元素,E为第三周期元素,所以B和C位于第二周期,E最外层电子数大于4而小于8,B的最外层电子数比E少1,B、E、F的最外层电子数之和为12,且这几种元素原子序数小于20,则符合条件的只有B是N、C是O、E是S、F是K元素,
(1)D、C形成的化合物是SiO2,在通讯上的重要用途是制作光导纤维,故答案为:光导纤维;
(2)E与F两元素可形成化合物为K2S,为离子化合物,用电子式表示其化合物的形成过程为 ,
,
故答案为: ;
;
(3)B是N元素、D是Si元素,硝酸能和硅酸钠反应生成硅酸,反应方程式为2HNO3+Na2SiO3=2NaNO3+H2SiO3,故答案为:2HNO3+Na2SiO3=2NaNO3+H2SiO3;
(4)C、F两元素形成原子个数比为1:1的化合物甲为K2O2,K2O2的电子式为 ,故答案为:
,故答案为: ;
;
(5)①空气有热胀冷缩的性质,将q插入水中,打开活塞,将分液漏斗中的液体滴入试管中,二者反应,如果q中有气体逸出就证明该反应是放热反应;
②氧气能使带火星的木条复燃,过氧化钾和水反应后,将带火星的木条放置在P口处,如果木条复燃,则说明有氧气生成,
故答案为:①将q插入水中,打开活塞,液体和固体反应过程中如果q中有气体逸出,说明该反应是放热反应;
②将带火星的木条放置在P口处,如果木条复燃,则说明有氧气生成.
D的次外层电子数是最外层电子数的两倍,D元素前有多种元素,所以D的次外层为L层,则D最外层电子式是4,则D是Si元素;
B和C、C和E分别相邻,且这几种元素都是短周期元素,E为第三周期元素,所以B和C位于第二周期,E最外层电子数大于4而小于8,B的最外层电子数比E少1,B、E、F的最外层电子数之和为12,且这几种元素原子序数小于20,则符合条件的只有B是N、C是O、E是S、F是K元素,
(1)D、C形成的化合物是SiO2,在通讯上的重要用途是制作光导纤维,故答案为:光导纤维;
(2)E与F两元素可形成化合物为K2S,为离子化合物,用电子式表示其化合物的形成过程为
 ,
,故答案为:
 ;
;(3)B是N元素、D是Si元素,硝酸能和硅酸钠反应生成硅酸,反应方程式为2HNO3+Na2SiO3=2NaNO3+H2SiO3,故答案为:2HNO3+Na2SiO3=2NaNO3+H2SiO3;
(4)C、F两元素形成原子个数比为1:1的化合物甲为K2O2,K2O2的电子式为
 ,故答案为:
,故答案为: ;
;(5)①空气有热胀冷缩的性质,将q插入水中,打开活塞,将分液漏斗中的液体滴入试管中,二者反应,如果q中有气体逸出就证明该反应是放热反应;
②氧气能使带火星的木条复燃,过氧化钾和水反应后,将带火星的木条放置在P口处,如果木条复燃,则说明有氧气生成,
故答案为:①将q插入水中,打开活塞,液体和固体反应过程中如果q中有气体逸出,说明该反应是放热反应;
②将带火星的木条放置在P口处,如果木条复燃,则说明有氧气生成.
点评:本题涉及物质的检验、电子式的书写、非金属性强弱的判断等知识点,正确推断元素是解本题关键,注意过氧化钾电子式的书写,为易错点.

练习册系列答案
相关题目
研究性学习小组为了证明铁的金属性比铜强,他设计了如下几种方案,其中合理的是 ( )
| A、铁片置于硫酸铜溶液中有铜析出 |
| B、铁、铜与氯气反应分别生成FeCl3、CuCl2 |
| C、铜片置于FeCl3溶液中,铜片逐渐溶解(2FeCl3+Cu=2FeCl2+CuCl2) |
| D、铁片、铜片分别置于盛有稀硫酸的烧杯中,铁片上有气泡产生,而铜片无气泡 |
| E、常温下,分别将铁片和铜片置于浓硝酸中,铁片不溶解,而铜片溶解 |
X、Y为两种元素的原子,X-与Y+具有相同的电子层结构,由此可知( )
| A、X的原子半径大于Y的原子半径 |
| B、X的电负性大于Y的电负性 |
| C、X-的半径大于Y+的半径 |
| D、X的第一电离能小于Y的第一电离能 |
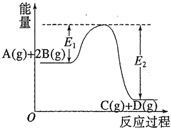 反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )
反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )| A、该反应是吸热反应 |
| B、当反应达到平衡时,升高温度,A的转化率增大 |
| C、反应体系中加入催化剂对反应热无影响 |
| D、在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 |
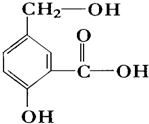 在某有机物A的分子中,具有酚羟基、醇羟基、羟基等官能团,其结构简式如图.
在某有机物A的分子中,具有酚羟基、醇羟基、羟基等官能团,其结构简式如图.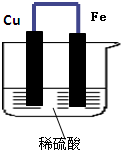 如图示的原电池中,
如图示的原电池中,
 和
和 