题目内容
 (1)0.4molNH4ClO4含有氧原子数为
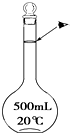
(1)0.4molNH4ClO4含有氧原子数为(2)某同学观察液面的情况如图所示,对所配溶液浓度将有何影响?
(3))若实验过程中出现如下情况应如何处理?加蒸馏水时不慎超过了刻度
考点:溶液的配制
专题:
分析:(1)0.4molNH4ClO4含有0.4mol×4=1.6mol氧原子,带入N=nNA计算;
(2)定容时俯视刻度线,导致所配溶液的液体偏小,浓度偏高;
(3)加蒸馏水时不慎超过了刻度,所配溶液浓度低,应重新配制.
(2)定容时俯视刻度线,导致所配溶液的液体偏小,浓度偏高;
(3)加蒸馏水时不慎超过了刻度,所配溶液浓度低,应重新配制.
解答:
解:(1)0.4molNH4ClO4含有0.4mol×4=1.6mol氧原子,氧原子的数目为1.6mol×NAmol-1=1.6NA,
故答案为:1.6NA;
(2)定容时俯视刻度线,导致所配溶液的液体偏小,浓度偏高,
故答案为:偏高;
(3)加蒸馏水时不慎超过了刻度,所配溶液浓度低,应重新配制,
故答案为:倒掉重配.
故答案为:1.6NA;
(2)定容时俯视刻度线,导致所配溶液的液体偏小,浓度偏高,
故答案为:偏高;
(3)加蒸馏水时不慎超过了刻度,所配溶液浓度低,应重新配制,
故答案为:倒掉重配.
点评:本题考查了配制一定物质的量浓度的溶液的方法及误差分析,题目难度不大,试题基础性强,该题的难点在于误差分析,需要明确的是根据c=
,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起.
| n |
| V |

练习册系列答案
相关题目
下列说法正确的是( )
| A、Cl2和SO2都能使石蕊试液和品红褪色 |
| B、实验室可用NaOH溶液处理NO2和HCl废气 |
| C、实验室可用浓硫酸干燥氨气 |
| D、Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒 |
已知S2O8n-离子和H2O2一样含有过氧键,因此也有强氧化性,S2O8n-离子在一定条件下可把Mn2+氧化成MnO4-离子,若反应后S2O8n-离子变成SO42-;又知反应中氧化剂与还原剂的离子数之比为5:2,则S2O8n-中的n值和S的化合价是( )
| A、2,+7 | B、2,+6 |
| C、4,+7 | D、4,+4 |
下列实验操作正确的是( )
A、 分液 |
B、 过滤 |
C、 转移溶液 |
D、 蒸馏 |
以下有关实验的叙述中,正确的是( )
| A、利用萃取分液操作分离汽油和CCl4 |
| B、用玻璃棒蘸取待测液,点在润湿的pH试纸上测定其pH |
| C、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| D、读取滴定管内液体的体积,俯视读数导致读数偏小 |
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)?
N2(g)+CO2(g)△H=-373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| 1 |
| 2 |
| A、加催化剂同时升高温度 |
| B、加催化剂同时增大压强 |
| C、升高温度同时充入N2 |
| D、降低温度同时增大压强 |
下列叙述错误的是( )
| A、钢铁表面发生吸氧腐蚀时,钢铁表面水膜的pH增大 |
| B、在镀件上电镀锌,可以用锌作阳极,也可以用惰性电极材料作阳极 |
| C、电解精炼铜时,同一时间内阳极溶解的铜的质量比阴极析出的铜的质量少 |
| D、工作时在原电池的负极和电解池的阳极上都是发生氧化反应 |