题目内容
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,22.4L乙醇中含有的碳原子数目为2NA |
| B、1mol CnH2n含有的共同电子对数为(3n+1)NA |
| C、1mol CO2与1mol Na2O2完全反应时,转移的电子数目为NA |
| D、1mol/L的FeCl3溶液中,所含Fe3+的数目小于NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下乙醇是液体;
B.1mol CnH2n含有的共同电子对数为3n;
C.2Na2O2+2CO2=2Na2CO3+O2↑,每反应2molCO2时反应中转移的电子为2mol;
D.Fe3+发生水解.
B.1mol CnH2n含有的共同电子对数为3n;
C.2Na2O2+2CO2=2Na2CO3+O2↑,每反应2molCO2时反应中转移的电子为2mol;
D.Fe3+发生水解.
解答:
解:A.标准状况下乙醇是液体,22.4L乙醇的物质的量不是1mol,故A错误;
B.1mol CnH2n含有的共同电子对数为3nNA,故B错误;
C.2Na2O2+2CO2=2Na2CO3+O2↑,每反应1molCO2时反应转移的电子数目为NA,故C正确;
D.Fe3+发生水解,Fe3+的数目小于NA,故D错误.
故选C.
B.1mol CnH2n含有的共同电子对数为3nNA,故B错误;
C.2Na2O2+2CO2=2Na2CO3+O2↑,每反应1molCO2时反应转移的电子数目为NA,故C正确;
D.Fe3+发生水解,Fe3+的数目小于NA,故D错误.
故选C.
点评:本题考查阿伏加德罗常数,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、99gD2O所含有的电子数为5NA |
| B、标准状况下,11.2LH2O含有的分子数为0.5NA |
| C、常温常压下,22g氧气和26g臭氧所含氧原子总数为3NA |
| D、O.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA |
 某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如图,下列说法不正确的是( )
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如图,下列说法不正确的是( )| A、A为电源正极 |
| B、阳极区溶液中发生的氧化还原反应为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
| C、阴极区附近溶液pH降低 |
| D、若不考虑气体的溶解,当收集到H213.44 L(标准状况)时,有0.1 mol Cr2O72-被还原 |
下列解释实验现象的反应方程式正确的是( )
| A、SO2通入到滴加酚酞的NaOH溶液中,红色变浅:SO2+2NaOH=Na2SO4+H2O | ||||
| B、向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72-+H2O?2CrO42-+2H+ | ||||
| C、等浓度的NH4Al(SO4)2溶液与Ba(OH)2溶液以1:2体积比混合出现白色沉淀:Al3++2SO42-+2Ba2++3OH-=2BaSO4↓+Al(OH)3↓ | ||||
D、铝热反应的原理为:Al2O3+2Fe
|
白云石的化学式是xCaCO3?yMgCO3.可用于制取耐火材料等,优质的白云石粉可作为昂贵的二氧化钛填料的替代品.现称取27.6g白云石,加热到质量不再变化,收集到的CO2为6.72L(已换算成标准状况).下列有关说法正确的是( )
| A、白云石的化学式为2CaCO3?MgCO3 |
| B、残留固体的质量为14.4g |
| C、取13.8g该白云石与足量盐酸完全反应,最多收集到标准状况下的CO22.24L |
| D、27.6g白云石与过量盐酸完全反应,可消耗HCl0.3mol |
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 物质 编号 |
物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| ① | 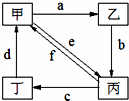 |
Cu | CuO | CuSO4 | Cu(NO3)2 |
| ② | Na2CO3 | NaOH | NaHCO3 | CO2 | |
| ③ | (NH4)2SO3 | CaSO3 | SO2 | NH4HSO3 | |
| ④ | CH3CH2Cl | C2H5OH | CH2=CH2 | CH3CH3 |
| A、①②③④ | B、①②③ |
| C、①③④ | D、②④ |
用盐酸中和相同体积、相同pH值的Ba(OH)2、NaOH和NH3?H2O三种稀溶液,所用相同浓度的盐酸体积分别为V1、V2和V3,则三者关系为( )
| A、V1>V2>V3 |
| B、V3=V2>V1 |
| C、V1=V2>V3 |
| D、V3>V2=V1 |
 下表中所示概念问的从属关系不符合如图所示的是( )
下表中所示概念问的从属关系不符合如图所示的是( )