题目内容
2.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C═2AlN+3CO①在化学方程式上用“双线桥法”标出该反应中电子转移的方向和数目.
②在该反应中,氧化剂是N2.
分析 Al2O3+N2+3C=2AlN+3CO中,N元素的化合价由0降低为-3价,C元素的化合价由0升高为+2价,该反应中转移6e-,以此来解答.
解答 解:①Al2O3+N2+3C=2AlN+3CO中,N元素的化合价由0降低为-3价,C元素的化合价由0升高为+2价,该反应中转移6e-,则电子转移的方向和数目为 ,故答案为:
,故答案为: ;
;
②N元素的化合价降低,则N2为氧化剂,故答案为:N2;
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意从元素化合价角度分析,侧重基本概念和转移电子数计算的考查,题目难度不大.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
13.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究.
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气.C(s)+H2O(g)?H2(g)+CO(g)△H=+131.3kJ•mol-1,△S=+133.7J•mol-1•K-1,
①该反应在低温下不能(填“能”或“不能”)自发进行.
②写出该反应的平衡常数表达式k=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$.
(2)已知在400℃时,N2(g)+3H2(g)?2NH3(g)的K=0.5.
①在400℃时,2NH3(g)?N2(g)+3H2(g)的K′=2(填数值).
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正= v(N2)逆(填“>”、“<”、“=”或“不能确定”).
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡向左移动(填“向左”、“向左”或“不”);使用催化剂,反应的△H不改变(填“增大”、“减小”或“不改变”).
(3)水煤气转化反应CO(g)+H2O(g)?CO2(g)+H2(g)在一定温度下达到化学平衡.现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如表两组教据:
①实验l中以CO2表示的反应速率为v(CO2)=0.16mol/(L•min);
②实验1的平衡常数K1大于实验2的平衡常数K2 (填“大于””小于,“等于”“不能确定”).
③该反应正方向为放 (填“吸”或‘放”)热反应.
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气.C(s)+H2O(g)?H2(g)+CO(g)△H=+131.3kJ•mol-1,△S=+133.7J•mol-1•K-1,
①该反应在低温下不能(填“能”或“不能”)自发进行.
②写出该反应的平衡常数表达式k=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$.
(2)已知在400℃时,N2(g)+3H2(g)?2NH3(g)的K=0.5.
①在400℃时,2NH3(g)?N2(g)+3H2(g)的K′=2(填数值).
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正= v(N2)逆(填“>”、“<”、“=”或“不能确定”).
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡向左移动(填“向左”、“向左”或“不”);使用催化剂,反应的△H不改变(填“增大”、“减小”或“不改变”).
(3)水煤气转化反应CO(g)+H2O(g)?CO2(g)+H2(g)在一定温度下达到化学平衡.现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如表两组教据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
②实验1的平衡常数K1大于实验2的平衡常数K2 (填“大于””小于,“等于”“不能确定”).
③该反应正方向为放 (填“吸”或‘放”)热反应.
10.下列离子方程式书写正确的是( )
| A. | 把Mg粉放入FeCl3溶液中:2Fe3++3Mg+6H2O=2Fe(OH)3↓+3 Mg2++3H2↑ | |
| B. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO?+SO2+H2O=CaSO3↓+2HClO | |
| C. | 氯化铝溶液中加入偏铝酸钠溶液:Al3++3AlO2-+6H2O=4Al(OH)3↓ | |
| D. | 碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
17.下列变化中,属于吸热反应的是( )
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓H2SO4稀释 ④KClO3分解制O2 ⑤生石灰跟水反应生成熟石灰⑥CaCO3高温分解 ⑦CO2+C═2CO ⑧Ba(OH)2•8H2O与固体NH4Cl混合 ⑨C+H2O(g)═CO+H2 ⑩Al与HCl反应.
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓H2SO4稀释 ④KClO3分解制O2 ⑤生石灰跟水反应生成熟石灰⑥CaCO3高温分解 ⑦CO2+C═2CO ⑧Ba(OH)2•8H2O与固体NH4Cl混合 ⑨C+H2O(g)═CO+H2 ⑩Al与HCl反应.
| A. | ①②④⑥⑦⑧⑨ | B. | ②④⑥⑦⑧⑨ | C. | ①④⑥⑧ | D. | ①②④⑧⑨ |
7.下列物质的水溶液能导电,但其本身属于非电解质的是( )
| A. | 液氯 | B. | 干冰 | C. | 酒精 | D. | 金属钠 |
12.设NA为阿伏伽德罗常数值,下列叙述不正确的是( )
| A. | 淀粉可用于酿酒 | |
| B. | 13g苯中含C-H键的数目是NA | |
| C. | 1mol的金刚石中含4NA根C-C键 | |
| D. | 标准状况下,11.2L甲烷和乙烯的混合物含氢原子数是2NA |
 2NO2 △H<0,反应中NO的转化率与温度的关系。图中标出a、b、c、 d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是
2NO2 △H<0,反应中NO的转化率与温度的关系。图中标出a、b、c、 d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是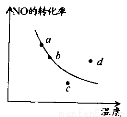

 X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )