题目内容
将24.4gNaOH固体溶于水配成100mL溶液,其密度为1.22g/mL
(1)该溶液中NaOH的物质的量浓度为 mol/L;
(2)该溶液中NaOH的质量分数为 ;
(3)从该溶液中取出10mL,含NaOH的物质的量为 mol;
(4)将取出的10mL溶液加水稀释到100mL,稀释后NaOH溶液的物质的量的浓度为 mol/L.
(1)该溶液中NaOH的物质的量浓度为
(2)该溶液中NaOH的质量分数为
(3)从该溶液中取出10mL,含NaOH的物质的量为
(4)将取出的10mL溶液加水稀释到100mL,稀释后NaOH溶液的物质的量的浓度为
考点:物质的量浓度的相关计算
专题:计算题
分析:根据n=
计算24.4gNaOH的物质的量,根据m=ρV计算溶液的质量,
(1)根据c=
计算NaOH溶液的物质的量的浓度;
(2)根据w=
×100%计算;
(3)溶液是均匀的,取出10mL溶液的物质的量浓度相等;该10mL溶液中NaOH物质的量为原溶液中的
;
(4)根据c=
计算稀释后NaOH溶液的物质的量的浓度.
| m |
| M |
(1)根据c=
| n |
| V |
(2)根据w=
| 溶质质量 |
| 溶液质量 |
(3)溶液是均匀的,取出10mL溶液的物质的量浓度相等;该10mL溶液中NaOH物质的量为原溶液中的
| 1 |
| 10 |
(4)根据c=
| n |
| V |
解答:
解:24.4gNaOH的物质的量为
=0.61mol,溶液质量为100mL×1.22g/mL=122g,
(1)该溶液中NaOH的物质的量浓度为
=6.1mol/L,故答案为:6.1;
(2)该溶液中NaOH的质量分数为
×100%=20%,故答案为:20%;
(3)溶液是均匀的,取出10mL溶液的物质的量浓度与原溶液相等,该10mL溶液中氢氧化钠的物质的量为原溶液中的
,为0.061mol,故答案为:0.061;
(4)取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为
=0.61mol/L,故答案为:0.61.
| 24.4g |
| 40g/mol |
(1)该溶液中NaOH的物质的量浓度为
| 0.61mol |
| 0.1L |
(2)该溶液中NaOH的质量分数为
| 24.4g |
| 122g |
(3)溶液是均匀的,取出10mL溶液的物质的量浓度与原溶液相等,该10mL溶液中氢氧化钠的物质的量为原溶液中的
| 1 |
| 10 |
(4)取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为
| 0.061mol |
| 0.1L |
点评:本题考查物质的量浓度、质量分数有关计算,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
下列关于氯水的叙述,不正确的是( )
| A、在一定浓度的氯水中加小苏打有气泡生成 |
| B、新制氯水中只存在2个平衡状态 |
| C、氯水应保存在棕色瓶中,久置的氯水,PH值减小 |
| D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |
下列过程或现象与盐类水解无关的是( )
| A、热的纯碱溶液去油污效果好 |
| B、配置FeCl3溶液时,加入少量HCl,以防止溶液浑浊 |
| C、水中加入明矾可以净化水 |
| D、实验室制氢气时往往在稀H2SO4中加少量的CuSO4可加快反应速率 |
常温下,某无色透明的溶液中,下列各组离子能够大量共存的是( )
| A、H+、Na+、Cl-、CO32- |
| B、Ba2+、Na+、SO42-、Cl- |
| C、MnO4-、K+、I-、H+ |
| D、Mg2+、Cl-、NO3-、H+ |
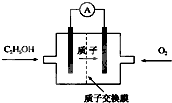 目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )| A、通入乙醇的电极为该电池的正极 |
| B、放电过程中,电源内部的H+从正极区向负极区迁移 |
| C、该电池的正极反应为:4H++O2+4e-=2H2O |
| D、用该电池做电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2 mol C2H5OH,阴极产生标准状况下气体的体积为13.44 L |
在离子浓度都为0.1mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是( )
| A、在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B、在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C、在含Fe3+、H+、NH4+的溶液中逐滴加入烧碱溶液:Fe3+、NH4+、H+ |
| D、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A、分散质粒子直径在1~100nm之间 |
| B、能透过半透膜 |
| C、呈红褐色 |
| D、都是透明的 |