��Ŀ����
4����1��0.1molij������������������ȫȼ�գ����ɵ�CO2��ˮ��0.6mol��������ķ���ʽΪC6H12����2������������ʹ��ˮ����������Һ��ɫ������һ�������£����Ժ�Һ�巢��ȡ����Ӧ����һ��ȡ����ֻ��һ�֣���������ڻ��������ṹ��ʽΪ
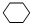 �������ǻ����飬�����Ķ��ȴ�����4�֣�
�������ǻ����飬�����Ķ��ȴ�����4�֣���3����������ʹ��ˮ��ɫ�������ڴ�����������H2�����ӳɷ�Ӧ������2��2-�������飬���������ϩ�����ṹ��ʽΪ��CH3��3C-CH=CH2��������3��3-����-1-��ϩ��
�˴Ź���������3�����շ壬���������9��1��2��
���������У��������Ϊͬϵ����ǣ�����ţ��٣���Ϊͬ���칹����Ǣۣ�
��CH3CH�TCHCH3������ ��CH2�TCHC��CH3��3
��CH3CH2CH�TCHCH2CH3�� �ܣ�CH3��2CH��CH2��2CH3��
���� ��1������CԪ�ء�HԪ���غ�ȷ�������ķ���ʽ��
��2�������Ͷ�Ϊ1������������ʹ��ˮ����������Һ��ɫ��˵�����б��������ͼ�������Ϊ������������һ�������£����Ժ�Һ�巢��ȡ����Ӧ����һ��ȡ����ֻ��һ�֣�������Ľṹ��ʽΪ ��
��
��3��������ʹ��ˮ��ɫ��˵�������к���1��C=C������������ϩ�����ڴ�����������H2�ӳ�����2��2-�������飨 ������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã�ȷ�������Ľṹ��ʽ��Ȼ�����ϩ��������ԭ���������������������õ��˴Ź����������շ�ĸ���������ȣ�ͬϵ���ǽṹ���ƣ�����������һ�������ɸ�CH2��ͬ���칹���Ƿ���ʽ��ͬ���ṹ��ͬ���ɴ˷������
������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã�ȷ�������Ľṹ��ʽ��Ȼ�����ϩ��������ԭ���������������������õ��˴Ź����������շ�ĸ���������ȣ�ͬϵ���ǽṹ���ƣ�����������һ�������ɸ�CH2��ͬ���칹���Ƿ���ʽ��ͬ���ṹ��ͬ���ɴ˷������
��� �⣺��1��n��������n��C����n��H��=n��������n��CO2����2n��H2O��=0.1mol��0.6mol��0.6mol��2=1��6��12����1�������к���6��Cԭ�ӡ�12��Hԭ�ӣ��ʸ����ķ���ʽΪ��C6H12��
�ʴ�Ϊ��C6H12��
��2�������ķ���ʽΪ��C6H12���䲻���Ͷ�Ϊ1������������ʹ��ˮ����������Һ��ɫ��˵�����б��������ͼ����ʸ���Ϊ����������һ��ȡ����ֻ��һ�֣�˵��������ֻ��һ��Hԭ�ӣ�����Ϊ�����飬�ṹ��ʽΪ�� ������ȴ������ڡ��䡢�Ժ�һ��̼��������ͬʱ��ȡ������4�֣��ʴ�Ϊ�����飻
������ȴ������ڡ��䡢�Ժ�һ��̼��������ͬʱ��ȡ������4�֣��ʴ�Ϊ�����飻 �������飻4��
�������飻4��
��3��������ʹ��ˮ��ɫ��˵�������к���1��C=C������������ϩ�����ڴ�����������H2�ӳ�����2��2-�������飨 ������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã������Ľṹ��ʽΪ����CH3��3CCH=CH2������Ϊ3��3-����-1-��ϩ����������3�������Ժ˴Ź���������3�����շ壬�����֮��Ϊ��9��1��2����Ϊͬϵ����Ǣ٣���Ϊͬ���칹����Ǣۣ��ʴ�Ϊ��ϩ����CH3��3C-CH=CH2�� 3��3-����-1-��ϩ��3��9��1��2���٣��ۣ�
������������̼ԭ�Ӷ�����Hԭ��ΪC=C˫��λ�ã������Ľṹ��ʽΪ����CH3��3CCH=CH2������Ϊ3��3-����-1-��ϩ����������3�������Ժ˴Ź���������3�����շ壬�����֮��Ϊ��9��1��2����Ϊͬϵ����Ǣ٣���Ϊͬ���칹����Ǣۣ��ʴ�Ϊ��ϩ����CH3��3C-CH=CH2�� 3��3-����-1-��ϩ��3��9��1��2���٣��ۣ�
���� ���⿼�����л������ʽ���ṹ��ʽ��ȷ������Ŀ�Ѷ��еȣ��������ճ����л���ṹ������Ϊ���ؼ���ע����ȷ�����غ���ȷ���л������ʽ�е�Ӧ�ã�

| A�� | ��Pt�缫���������MgC12��Һ��2H2O+2Cl- $\frac{\underline{\;ͨ��\;}}{\;}$H2��+C12��+2OH- | |
| B�� | ������Һ�м���Ba��OH��2��Һ�����ɵij�����������ࣺAl3++2SO42-+2Ba2++4OH-�TAlO2-+2BaSO4��+2H2O | |
| C�� | ����4 mol FeBr2����Һ��ͨ��3 mol Cl2��ַ�Ӧ��2Fe2++4Br-+3Cl2�T4Fe3++6Cl-+Br2 | |
| D�� | ̼������ڴ����У�CaCO3+2H+�TCa2++CO2��+H2O |
��NaOH����SiO2����NH4Cl���ܽ��ʯ����NaCl �ް��ף�
| A�� | �٢ۢ� | B�� | �٢ڢ� | C�� | �ڢܢ� | D�� | �ۢܢ� |

��֪�������������������pH
| Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
| ��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
| ��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
�ش��������⣺
��1�������ʵ����̿�ʹ��ǰ�轫����飬��ҪĿ��������Ӵ��������߷�Ӧ���ʣ������ܽ�MnCO3�Ļ�ѧ����ʽ��MnCO3+2HCl=MnCl2+CO2��+H2O��
��2������Һ1�м���˫��ˮʱ����Ӧ�����ӷ���ʽ��2Fe2++H2O2+4H2O=2Fe��OH��3��+4H+��
��3����Һ2�м����Թ��������ܵ����MnS���Գ�ȥCu2+����Ӧ�����ӷ���ʽ��MnS+Cu2+=Mn2++CuS��
��4����MnCl2ת��ΪMnO2��һ�ַ���������������������������ữ��NaClO3��Һ��MnCl2�������÷�Ӧ�����ӷ���ʽΪ����Mn2++��ClO3-+��4H2O=��Cl2��+��5MnO2+��8H+��
��5����MnCl2ת��ΪMnO2����һ�ַ����ǵ�ⷨ��
������MnO2�ĵ缫��Ӧʽ��Mn2+-2e-+2H2O=MnO2+4H+��
����ֱ�ӵ��MnCl2��Һ������MnO2��ͬʱ���������Cl2������Cl2�IJ����ǽ���ʪ�ĵ��۵⻯����ֽ������������������ֽ������֤����Cl2���ɣ�
����������MnCl2��Һ�м���һ������Mn��NO3��2��ĩ������Cl2��������ԭ�����������������£�����Mn2+Ũ��[������c��Mn2+��/c��Cl-��]��������Mn2+�ŵ磨������Cl-�ŵ磩��

 CH3COOC2H5+H2O��
CH3COOC2H5+H2O��