题目内容
14. 已知如表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.
已知如表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.| CH2COOH | HClO | H2CO2 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
(2)a、b、c三点中,水的电离程度由大到小的顺序是c>a>b(用编号表示).
(3)25℃时,NaClO溶液的水解平衡常数Kh=3.3×10-7molL-1.
(4)25℃时,NaHCO3溶液存在水解平衡,写出其水解的离子方程式HCO3-+H2O≒H2CO3+OH-
(5)0.1mol/L Na2CO3溶液中c(OH)-c(H+)=c(HCO3-)+2c(H2CO3).(用含c(HCO${\;}_{3}^{-}$),c(H2CO3)的关系式表示).
分析 (1)pH相等的CH3COOH、HClO,稀释相同的倍数时,较强酸中氢离子浓度小于较弱酸,则较弱酸的pH小于较强酸,酸中离子浓度越大则酸溶液的导电性越强;
(2)酸溶液中氢离子浓度越小,酸抑制水电离程度越小;
(3)NaClO的水解平衡常数Kh=$\frac{c(HClO)•c(O{H}^{-})}{c(Cl{O}^{-})}$=$\frac{Kw}{Ka(HClO)}$;
(4)NaHCO3水解生成碳酸和氢氧化钠;
(5)根据电荷守恒和物料守恒分析.
解答 解:(1)据电离平衡常数可知,醋酸的酸性比次氯酸强,pH相等的CH3COOH、HClO,稀释相同的倍数时,较强酸中氢离子浓度小于较弱酸,所以曲线Ⅰ表示的酸是CH3COOH;
故答案为:CH3COOH;
(2)酸溶液中氢离子浓度越小,酸抑制水电离程度越小,a、b、c三点溶液中C(H+)大小顺序是b>a>c,所以水电离程度c>a>b,
故答案为:c>a>b;
(3)NaClO的水解平衡常数Kh=$\frac{c(HClO)•c(O{H}^{-})}{c(Cl{O}^{-})}$=$\frac{Kw}{Ka(HClO)}$=$\frac{1.0×1{0}^{-14}}{3.0×1{0}^{-8}}$=3.3×10-7molL-1;
故答案为:3.3×10-7molL-1;
(4)NaHCO3水解生成碳酸和氢氧化钠,其水解离子方程式为:HCO3-+H2O≒H2CO3+OH-;
故答案为:HCO3-+H2O≒H2CO3+OH-;
(5)0.1mol/L Na2CO3溶液中电荷守恒为:c(OH)+c(HCO3-)+2c(CO32-)=c(H+)+c(Na+),物料守恒为:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3);则c(OH)-c(H+)=c(HCO3-)+2c(H2CO3);
故答案为:c(HCO3-)+2c(H2CO3).
点评 本题考查离子浓度大小的比较,侧重于弱电解质的电离的考查,题目难度中等,根据酸的电离常数与酸根离子水解程度、酸的酸性强弱等知识点来分析解答.

| A. | 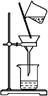 除去粗盐溶液中的不溶物 | B. |  碳酸氢钠受热分解 | ||
| C. | 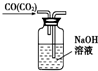 除去CO气体中的CO2气体 | D. | 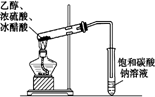 乙酸乙酯制备演示实验 |
(一)甲同学设计了以下实验检测该补铁药品中是否含有Fe2+并探究Vc的作用:

(二)乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为5Fe2++8H++MnO-4═5Fe3++Mn2++4H2O.准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用 0.020mol/L的KMnO4溶液滴定,用去KMnO4溶液记录如下:
| 待测液 体积(mL) | 标准液 | |||||
| 浓度(mol/L) | 滴定前 | 滴定后 | 体积(mL) | 平均值(mL) | ||
| 第一次 | 20.00 | 0.0200 | 0.00 | 14.30 | ||
| 第二次 | 0.20 | 12.22 | ||||
| 第三次 | 0.00 | 11.98 | ||||
(2)该药品含“铁”的含量是33.6%(填数值,不需计算过程)
(3)该实验中的试剂2与甲同学设计的实验中的试剂1都可以是C(填编号)
A.蒸馏水 B.稀盐酸 C.稀硫酸 D.稀硝酸
(4)本实验滴定过程中滴定管需用高锰酸钾标准溶液润洗,其操作方法是在酸式滴定管中加入1-2mLKMnO4溶液,将滴定管横过来并转动,让KMnO4溶液浸过滴定管内壁,从下面放掉浸洗液,重复操作2-3次.
操作滴定管的图示正确的是A(填编号)
(5)某同学做用标准NaOH溶液滴定HCl溶液测定其浓度,下列不当操作会导致实验结果偏高的是df
a.酸式滴定管在装酸液前未用待测盐酸溶液润洗.
b.开始实验时碱式滴定管尖嘴部分没有气泡,滴定结束生成气泡
c.锥形瓶内溶液颜色变化由无色变为粉红色,立即记下滴定管液面所在刻度.
d.盛待测溶液的锥形瓶滴定前用待测液液润洗.
e.锥形瓶在装盐酸后,又加了少量蒸馏水后滴定.
f.若用含少量NaCl的NaOH固体配制标准溶液用来滴定上述盐酸.
 某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:
某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如图所示:已知①A、B、C、D、G含有同种元素.
②
| 纯A(单质) | B溶液 | D固体 | G溶液 | |
| 颜色 | 银白色 | 棕黄色 | 红棕色 | 浅绿色 |
依据以上信息填空:
(1)写出D的化学式:Fe2O3.
(2)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色,写出该变化的化学方程式FeSO4+NaOH=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(3)写出反应A转化为B的化学方程式:2Fe+3Cl2=2FeCl3.
(4)B→F的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.如何检验该反应生成的金属阳离子,简述操作方法及现象取反应后溶液少量滴入酸性高锰酸钾,若紫红色褪去,或滴入铁氰化钾生成蓝色沉淀即证明生成Fe2+离子.
| A. | 消除硫酸厂尾气排放:SO2+2NH3+H2O═(NH4)2SO3 | |
| B. | 消除制硝酸工业尾气的氮氧化物污染:NO+NO2+2NaOH═2NaNO2+H2O | |
| C. | 制CuSO4:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O | |
| D. | 制CuSO4:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO CuO+H2SO4(稀)═CuSO4+H2O |
| A. | 用酒精萃取碘水中的碘 | |
| B. | 海盐经过溶解、过滤、蒸发制纯净的NaCl | |
| C. | CO2气体混有少量HCl气体,将气体通过盛有饱和Na2CO3中溶液的洗气瓶以除去HCl气体 | |
| D. | 分液操作时,分液漏斗中先把下层液体从下口放出,再把上层液体从上口倒出 |
 钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+
钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+16H+