题目内容
下列关于铁矿石的说法正确的是( )
| A、赤铁矿的主要成分是Fe3O4 |
| B、铁矿石的主要成分与铁锈的主要成分相同 |
| C、磁铁矿粉末溶于盐酸后,加入KSCN溶液,溶液变血红色 |
| D、FeO俗称铁红 |
考点:铁的氧化物和氢氧化物,二价Fe离子和三价Fe离子的检验
专题:
分析:A、赤铁矿的成分是氧化铁,化学式为:Fe2O3;
B、赤铁矿成分主要是氧化铁,铁锈主要成分也是氧化铁;
C、磁铁矿是Fe3O4,溶液稀盐酸生成三价铁;
D、氧化铁俗称铁红,据此解答即可.
B、赤铁矿成分主要是氧化铁,铁锈主要成分也是氧化铁;
C、磁铁矿是Fe3O4,溶液稀盐酸生成三价铁;
D、氧化铁俗称铁红,据此解答即可.
解答:
解:A、赤铁矿的成分是氧化铁,化学式为:Fe2O3,故A错误;
B、赤铁矿成分主要是氧化铁,铁锈主要成分也是氧化铁,故B正确;
C、磁铁矿是Fe3O4,溶液稀盐酸生成三价铁,离子反应方程式为:Fe3O4+8H+=Fe2++2Fe3++4H2O,故加入KSCN溶液显红色,故C正确;
D、氧化铁俗称铁红,故D错误,故选BC.
B、赤铁矿成分主要是氧化铁,铁锈主要成分也是氧化铁,故B正确;
C、磁铁矿是Fe3O4,溶液稀盐酸生成三价铁,离子反应方程式为:Fe3O4+8H+=Fe2++2Fe3++4H2O,故加入KSCN溶液显红色,故C正确;
D、氧化铁俗称铁红,故D错误,故选BC.
点评:本题主要考查的是铁的氧化物与其俗名、铁的氧化物的性质等,难度中等.

练习册系列答案
相关题目
某校活动小组为探究金属腐蚀的相关原理,设计了如图a所示装置,图a的铁棒末段分别连上一块Zn片和Cu片,并静置于含有K3Fe(CN)6及酚酞的混合凝胶上.一段时间后发现凝胶的某些区域(如图b示)发生了变化,已知Fe2+可用K3Fe(CN)6来检验(呈蓝色).则下列说法不正确的是( )


| A、甲区呈现红色 |
| B、乙区产生Zn2+ |
| C、丙区发生的电极反应式:Cu-2e-=Cu2+ |
| D、丁区呈现蓝色 |
设阿伏加德罗常数为NA,下列说法正确的是( )
| A、1 mol Cl2与足量Fe反应,转移的电子数为3NA |
| B、常温常压下,14g氮气中含有 NA个原子 |
| C、标准状况下,22.4L水中含有的原子数为3NA |
| D、在25℃、101 kPa时,22.4 L氢气中含有NA个氢分子 |
下列关于铜电极的叙述中不正确的是( )
| A、铜锌原电池中铜是正极 |
| B、在镀件上镀铜时可以用金属铜作阳极 |
| C、用电解法精炼粗铜时粗铜作阴极 |
| D、镀铜的铁器,若发生缺损易形成以铜为正极的原电池 |
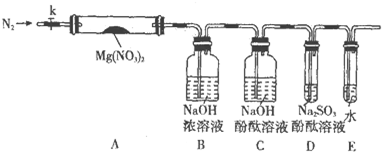 固体硝酸盐加热易分解且产物较复杂.已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐的热分解反应方程式如下:
固体硝酸盐加热易分解且产物较复杂.已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐的热分解反应方程式如下: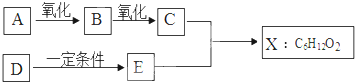
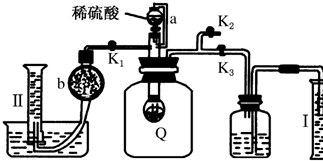 为测定保存在干燥环境中已部分变质的过氧化钠样品(只有一种杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开漏斗的活塞,将稀硫酸滴入气球中.
为测定保存在干燥环境中已部分变质的过氧化钠样品(只有一种杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开漏斗的活塞,将稀硫酸滴入气球中.
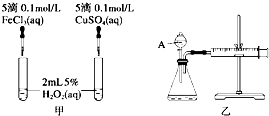 经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验.回答相关问题:
经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验.回答相关问题: