ЬтФПФкШн
ЁОЬтФПЁПМзДМ(CH3OH)ЪЧвЛжжПЩдйЩњФмдДЃЌОпгаЙуЗКЕФПЊЗЂКЭгІгУЧАОАЁЃ
ЃЈ1ЃЉвбжЊдкГЃЮТГЃбЙЯТЃК
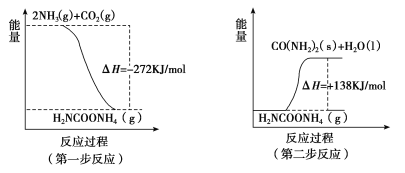
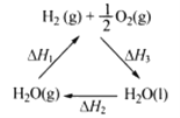
Ђй 2CH3OH(l) ЃЋ 3O2(g) ЃН 2CO2(g) ЃЋ 4H2O(g) ІЄH ЃНЃ1275.6 kJЃЏmol
Ђк 2CO (g)+ O2(g) ЃН 2CO2(g) ІЄH ЃНЃ566.0 kJЃЏmol
Ђл H2O(g) ЃН H2O(l) ІЄH ЃНЃ44.0 kJЃЏmol
ЧыМЦЫу1 molМзДМВЛЭъШЋШМЩеЩњГЩ1 molвЛбѕЛЏЬМКЭвКЬЌЫЎЗХГіЕФШШСПЮЊ________
ЃЈ2ЃЉФГЪЕбщаЁзщвРОнМзДМШМЩеЕФЗДгІдРэЃЌЩшМЦШчгвЭМЫљЪОЕФЕчГизАжУЁЃ
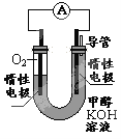
ЂйЙЄзївЛЖЮЪБМфКѓЃЌВтЕУШмвКЕФpH ЁЃ(ЬюЁАдіДѓЁБЁАМѕаЁЁБЁАВЛБфЁБ)
ЂкИУЕчГиИКМЋЕФЕчМЋЗДгІЮЊ ЁЃ
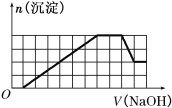
ЃЈ3ЃЉФГН№ЪєЕФЯрЖддзгжЪСПЮЊ52.00ЃЌгУЩЯЪіЕчГиЕчНтИУН№ЪєЕФвЛжжКЌбѕЫсбЮЕФЫсадЫЎШмвКЪБЃЌбєМЋУПЗХГі3 360 mL(БъзМзДПі)бѕЦјЃЌвѕМЋЮіГіН№Ъє10.4 gЃЌдкИУКЌбѕЫсбЮжаН№ЪєЕФЛЏКЯМлЮЊ ЃЌ
дкИУЪЕбщжаЃЌШєВЛПМТЧФмСПЕФЫ№ЪЇЃЌЕчГижаЯћКФМзДМЕФжЪСПзюЩйЪЧ g(НсЙћОЋШЗжС0.1 g)
ЁОД№АИЁП
ЃЈ1ЃЉ442.8KJ
ЃЈ2ЃЉМѕаЁЃЌCH3OH ЈC 6eЃ + 8OHЁЊ === CO32Ѓ +6H2O
ЃЈ3ЃЉ+3ЃЛ3.2
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКЃЈ1ЃЉЂй2CH3OH(l)+3O2(g)ЈT2CO2(g)+4H2O(g)ЁїH=-1275.6kJmol-1ЃЌЂк2CO(g)+O2(g)ЈT2CO2(g) ЁїH=-566.0kJmol-1ЃЌЂлH2O(g)ЈTH2O(l)ЁїH=-44.0kJmol-1ЃЌИљОнИЧЫЙЖЈТЩЃЌНЋвбжЊЗДгІ![]() ЁС(Ђй-Ђк+ЂлЁС4)ЕУЕНCH3OH(l)+O2(g)=CO(g)+2H2O(l)ЃЌЫљвдИУЗДгІЕФЁїH=
ЁС(Ђй-Ђк+ЂлЁС4)ЕУЕНCH3OH(l)+O2(g)=CO(g)+2H2O(l)ЃЌЫљвдИУЗДгІЕФЁїH=![]() ЁС[(-1275.6kJ/mol)-(-566.0kJ/mol)+ (-44.0kJ/mol)ЁС4] =-442.8kJmol-1ЃЌМДCH3OH(l)+O2(g) =CO(g)+ 2H2O(l) ЁїH=-442.8kJmol-1ЃЌвђДЫ1molМзДМВЛЭъШЋШМЩеЩњГЩ1molвЛбѕЛЏЬМКЭвКЬЌЫЎЗХГіЕФШШСПЮЊ442.8kJЃЌЙЪД№АИЮЊЃК442.8kJЃЛ
ЁС[(-1275.6kJ/mol)-(-566.0kJ/mol)+ (-44.0kJ/mol)ЁС4] =-442.8kJmol-1ЃЌМДCH3OH(l)+O2(g) =CO(g)+ 2H2O(l) ЁїH=-442.8kJmol-1ЃЌвђДЫ1molМзДМВЛЭъШЋШМЩеЩњГЩ1molвЛбѕЛЏЬМКЭвКЬЌЫЎЗХГіЕФШШСПЮЊ442.8kJЃЌЙЪД№АИЮЊЃК442.8kJЃЛ
ЃЈ2ЃЉЂйCH3OH+8OH--6e-=CO32-+6H2OЃЌЧтбѕИљРызгБЛЯћКФЃЌЫљвдШмвКЕФpHМѕаЁЃЌЙЪД№АИЮЊЃКМѕаЁЃЛ
ЂкдкШМСЯЕчГижаЃЌИКМЋЪЧШМСЯЗЂЩњЪЇЕчзгЕФбѕЛЏЗДгІЃЌМДCH3OH+8OH--6e-=CO32-+6H2OЃЌЙЪД№АИЮЊЃКCH3OH+8OH--6e-=CO32-+6H2OЃЛ
ЃЈ3ЃЉЩшН№ЪєЕФЛЏКЯМлЮЊxЃЌдђИљОнЕУЪЇЕчзгЪиКуЙиЯЕПЩЕУ![]() ЁС4=
ЁС4=![]() ЁСxЃЌНтЕУx=3ЃЌ
ЁСxЃЌНтЕУx=3ЃЌ
n(O2)=![]() =0.15molЃЌЕУЕН0.15molЁС4=0.6molЕчзгЃЌгЩCH3OH+8OH--6e-=CO32-+6H2OПЩжЊЃЌ0.1molМзДМЪЇШЅ0.6molЕчзгЃЌвђДЫМзДМЕФжЪСПЮЊ0.1molЁС32g/mol=3.2gЃЌЙЪД№АИЮЊЃК+3ЃЛ3.2ЁЃ
=0.15molЃЌЕУЕН0.15molЁС4=0.6molЕчзгЃЌгЩCH3OH+8OH--6e-=CO32-+6H2OПЩжЊЃЌ0.1molМзДМЪЇШЅ0.6molЕчзгЃЌвђДЫМзДМЕФжЪСПЮЊ0.1molЁС32g/mol=3.2gЃЌЙЪД№АИЮЊЃК+3ЃЛ3.2ЁЃ

 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИ