题目内容
11.在海轮的船壳上连接锌块,下列相关说法正确的是( )| A. | 制成合金保护船体 | B. | 是外加电流的阴极保护法 | ||
| C. | 船体的反应:Fe-2e→Fe2+ | D. | 锌块的反应:Zn-2e→Zn2+ |
分析 在海轮的船壳上连接锌块,则船体、锌和海水构成原电池,船体做正极,锌块做负极,海水做电解质溶液,据此分析.
解答 解:在海轮的船壳上连接锌块,则船体、锌和海水构成原电池,船体做正极,锌块做负极,海水做电解质溶液.
A、在海轮的船壳上连接锌块是形成原电池来保护船体,而非合金,故A错误;
B、在海轮的船壳上连接锌块是形成原电池来保护船体,锌做负极被腐蚀,船体做正极被保护,是牺牲阳极的阴极保护法,故B错误;
C、船体做正极被保护,溶于海水的氧气放电:O2+4e-+2H2O=4OH-,故C错误;
D、锌做负极被腐蚀:Zn-2e→Zn2+,故D正确.
故选D.
点评 本题考查了金属的电化学腐蚀和防护,难度不大,应注意的是在船体上连接的锌块做负极.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
2.一定条件下,反应N2(g)+3H2(g)?2NH3(g)在10L的密闭容器中进行,测得2min内N2的物质的量由20mol减小到8mol,则2min内用NH3表示的反应速率为( )
| A. | 1.2mol/(L•min) | B. | 6.0mol/(L•min) | C. | 0.6mol/(L•min) | D. | 0.4mol/(L•min) |
19.材料在生产和日常生活中有着广泛的应用.下列叙述正确的是( )
| A. | 玻璃钢是复合材料 | B. | 铝是黑色金属材料 | ||
| C. | 石英是半导体材料 | D. | 水泥是新型无机非金属材料 |
6.不能用于比较Na与Al金属性相对强弱的事实是( )
| A. | Na和AlCl3溶液反应 | B. | 最高价氧化物对应水化物的碱性 | ||
| C. | 单质与H2O反应的难易程度 | D. | 同浓度NaCl和AlCl3溶液的pH |
3.25℃时,下列叙述正确的是( )
| A. | 将pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7 | |
| B. | NH4HSO4溶液中滴加NaOH溶液至pH=7,则c(Na+)=2c(SO42-) | |
| C. | 0.1 mol•L-1CH3COOH溶液与0.1 mol•L-1CH3COONa等体积混合后pH<7,则c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| D. | KNO3和CH3COONH4溶液pH均为7,两溶液中水的电离程度相同 |
20.某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取
实验(一) 碘含量的测定
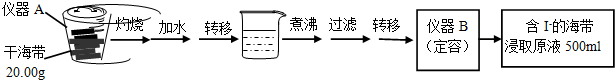
取0.0100mol•Lˉ1的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量.测的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
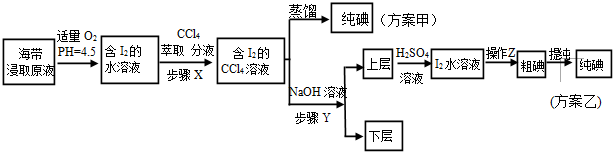
已知:3I2+6NaOH═5NaI+NaIO3+3H2O,请回答:
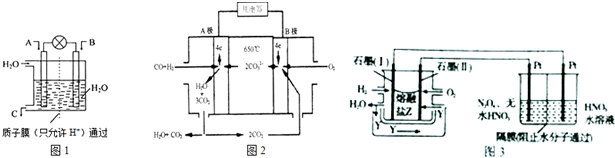
(1)实验(一) 中的仪器名称:仪器A坩埚,仪器 B500mL容量瓶.
(2)该次滴定终点时用去AgNO3溶液的体积为20.00mL,计算得海带中碘的百分含量为0.635%.
(3)①分液漏斗使用前须检漏.
②步骤X中,萃取后分液漏斗内观察到的现象是液体分为上下两层,下层呈紫红色.
③下列有关步骤Y的说法,正确的是AB.
A.应控制NaOH溶液的浓度和体积 B.将碘转化呈离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D.NaOH溶液可以由乙醇代替
(4)方案甲中采用蒸馏不合理,理由是碘单质易升华,会导致碘损失.
实验(一) 碘含量的测定

取0.0100mol•Lˉ1的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量.测的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
另制海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH═5NaI+NaIO3+3H2O,请回答:
(1)实验(一) 中的仪器名称:仪器A坩埚,仪器 B500mL容量瓶.
(2)该次滴定终点时用去AgNO3溶液的体积为20.00mL,计算得海带中碘的百分含量为0.635%.
(3)①分液漏斗使用前须检漏.
②步骤X中,萃取后分液漏斗内观察到的现象是液体分为上下两层,下层呈紫红色.
③下列有关步骤Y的说法,正确的是AB.
A.应控制NaOH溶液的浓度和体积 B.将碘转化呈离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D.NaOH溶液可以由乙醇代替
(4)方案甲中采用蒸馏不合理,理由是碘单质易升华,会导致碘损失.