题目内容
已知NH3?H2O的电离方程式为NH3?H2O?NH4++OH-.在氨水中加入下列物质,氨的电离平衡及平衡时物质的浓度的变化:
(1)向氨水中加入硝酸铵固体,电离平衡 移动(填“向左”“向右”或“不”,下同);c(OH-) .(填“增大”“减小”或“不变”,下同)
(2)向氨水中加入氢氧化钾固体,电离平衡 移动;c(NH3?H2O) .
(3)向氨水中加入水,c(H+) .
(1)向氨水中加入硝酸铵固体,电离平衡
(2)向氨水中加入氢氧化钾固体,电离平衡
(3)向氨水中加入水,c(H+)
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氨水中存在下列平衡:NH3+H2O?NH3?H2O?NH4++OH-,如果加入能和铵根离子或氢氧根离子反应的物质,平衡就向电离方向移动,如果加入的物质中含有铵根离子或氢氧根离子,平衡向逆反应方向移动,加水稀释,减小减弱,据此分析解答.
解答:
解:氨水中存在下列平衡:NH3+H2O?NH3?H2O?NH4++OH-,如果加入能和铵根离子或氢氧根离子反应的物质,平衡就向电离方向移动,如果加入的物质中含有铵根离子或氢氧根离子,平衡向逆反应方向移动,加水稀释,减小减弱,
(1)向氨水中加入硝酸铵固体,铵根离子浓度增大,平衡逆向移动,氢氧根离子浓度减小,故答案为:向左;减小;
(2)向氨水中加入氢氧化钾固体,氢氧根离子浓度增大,平衡逆向移动,一水合氨浓度增大,故答案为:向左;增大;
(3)向氨水中加入水,氨水减小减弱,氢离子浓度增大,故答案为:增大.
(1)向氨水中加入硝酸铵固体,铵根离子浓度增大,平衡逆向移动,氢氧根离子浓度减小,故答案为:向左;减小;
(2)向氨水中加入氢氧化钾固体,氢氧根离子浓度增大,平衡逆向移动,一水合氨浓度增大,故答案为:向左;增大;
(3)向氨水中加入水,氨水减小减弱,氢离子浓度增大,故答案为:增大.
点评:本题考查了电离平衡的移动,根据勒夏特列原理进行分析解答即可,难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
某烃结构简式如图,则该有机物应命名为( )
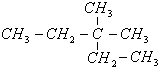
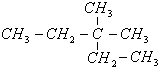
| A、2-甲基-2-乙基丁烷 |
| B、3-甲基-3-乙基己烷 |
| C、2,2-二甲基戊烷 |
| D、3,3-二甲基戊烷 |
某无色透明的碱性溶液中,能大量共存的离子组是( )
| A、Na+、H+、SO42-、HCO3- |
| B、Cu2+、K+、SO42-、NO3- |
| C、Na+、K+、Cl-、NO3- |
| D、Mg2+、K+、SO42-、Cl- |
某烃在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是( )
| A、分子中C、H个数比为1:2 |
| B、分子中的C、H的个数比为2:1 |
| C、该有机物的相对分子质量为14 |
| D、该烃常温下是气体 |
下列说法正确的是( )
| A、根据溶液中有CH3COOH、CH3COO-和H+即可证明CH3COOH达到电离平衡状态 |
| B、根据溶液中CH3COO-和H+的物质的量浓度相等即可证明CH3COOH达到电离平衡状态 |
| C、当NH3?H2O达到电离平衡时,溶液中NH3?H2O、NH4+和OH-的浓度相等 |
| D、H2CO3是分步电离的,电离程度依次减弱 |
常温下测得某无色溶液中由水电离出c(H+)为10-13mol/L,该溶液中一定能大量共存的离子组是( )
| A、K+、Na+、NO3-、SO42- |
| B、K+、Na+、Cl-、CO32- |
| C、Mg2+、K+、NO3-、Cl- |
| D、Fe2+、NO3-、SO42-、NH4+ |
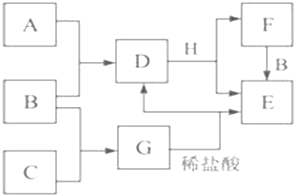 A-H分别是中学化学中的常见物质,它们之间有下图所示关系(反应中所需要和所生成的水均没有列出),已知B、H为常见的金属单质,A、C均为气体单质且A气体的颜色为黄绿色,F的水溶液为蓝色,B、D、G、E中均含同一种元素.请回答:
A-H分别是中学化学中的常见物质,它们之间有下图所示关系(反应中所需要和所生成的水均没有列出),已知B、H为常见的金属单质,A、C均为气体单质且A气体的颜色为黄绿色,F的水溶液为蓝色,B、D、G、E中均含同一种元素.请回答: