题目内容
青蒿酸的结构简式如图所示。下列有关说法正确的是( )
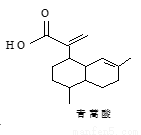
A.青蒿酸的分子式为C15H20O2
B.1mol青蒿酸最多可与3molH2加成
C.青蒿酸与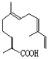 互为同分异构体
互为同分异构体
D.苯环上连有-CHO和-OH、分子中有6种不同化学环境氢的青蒿酸的同分异构体只有2种
练习册系列答案
相关题目
9.如图所示装置,电流计的指针发生偏转,正极产生气泡,负极变细,符合这种情况的是( )
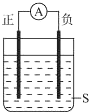

| A. | 正极Cu,负极Al,S为浓HNO3 | B. | 正极Ag,负极Al,S为NaOH | ||
| C. | 正极Ag,负极Cu,S为浓HCl | D. | 正极Zn,负极Cu,S为H2SO4 |
7.短周期元素X、Y、Z、W、R的原子序数依次增大,X单质在暗处与H2剧烈化合并发生爆炸,Y位于第IA族,Z所处的周期序数与族序数相等,W元素最高正价与最低负价和为0,R与X同族,则下列说法正确的是( )
| A. | 原子半径:Z>Y>X | |
| B. | X与R的核电荷数相差8 | |
| C. | 最高价氧化物对应的水化物的酸性:X>R | |
| D. | Y与Z两者最高价氧化物对应的水化物互不反应 |
1.烟气中含夺SCX夺大量有害的物质,烟气除硫的方法有多种,其中石灰石法烟气除硫工艺的主要反应如下:
I CaCO3 (s)?CO2 (g)+CaO(s)△H=+178kJ/mol
ⅡSO2(g)+CaO(s)?CaSO3(s)△H=-402kJ/mol
Ⅲ2CaS03(S)+02 (g)+4H2O(I)?2(CaS04•2H2O](S)△H=-234.2kJ/mol
(1)试写出由石灰石、二氧化硫、氧气和水反应生成生石膏的热化学方程式2SO2(g)+2CaS03(s)+02(g)+4H2O(l)=2[CaS04•2H2O](s)△H=-681.8kJ/mol.
(2)反应Ⅱ为烟气除硫的关健,取相同用量的反应物在3种不网的容器中进行该反应,A容器保持恒温恒压,B容器保持恒温恒容,C容器保持恒容絶热,且初始时3个容器的容积和温度均相同,下列说法正确的是ad.
a.3个容器中SO2的平衡转化率的大小顺序为 aA>aB>aC.
b.当A容器内气体的平均摩尔质量不变时,说明谈反应处于化学平衡状态
c.A、B两个容器达到平衡所用的时间:tA>tB
d.当C容器内平衡常数不变时,说明该反应处于化学平衡状态
(3)依据上述反应Ⅱ来除硫,将一定量的烟气压缩到一个20L的容器中,测得不同温度下,容器内SO2的质量(mg)如下表:
①在T1温度下,计算20〜40min内SO2的反应速率2×10-5mol/(L•min)
②若其它条件都相同T1< T2,《填“>”、“<”或“=”下同);x>0.06.
③在T2温度下,若平衡后将容器的容器压缩为10L,则新平衡时SO2的浓度平衡时SO2的浓度=(填“>”、“C”或“=”)理由是该反应的平衡常数表达式为K=$\frac{1}{c(S{O}_{2})}$,温度不变,K不变,所以浓度相等.
I CaCO3 (s)?CO2 (g)+CaO(s)△H=+178kJ/mol
ⅡSO2(g)+CaO(s)?CaSO3(s)△H=-402kJ/mol
Ⅲ2CaS03(S)+02 (g)+4H2O(I)?2(CaS04•2H2O](S)△H=-234.2kJ/mol
(1)试写出由石灰石、二氧化硫、氧气和水反应生成生石膏的热化学方程式2SO2(g)+2CaS03(s)+02(g)+4H2O(l)=2[CaS04•2H2O](s)△H=-681.8kJ/mol.
(2)反应Ⅱ为烟气除硫的关健,取相同用量的反应物在3种不网的容器中进行该反应,A容器保持恒温恒压,B容器保持恒温恒容,C容器保持恒容絶热,且初始时3个容器的容积和温度均相同,下列说法正确的是ad.
a.3个容器中SO2的平衡转化率的大小顺序为 aA>aB>aC.
b.当A容器内气体的平均摩尔质量不变时,说明谈反应处于化学平衡状态
c.A、B两个容器达到平衡所用的时间:tA>tB
d.当C容器内平衡常数不变时,说明该反应处于化学平衡状态
(3)依据上述反应Ⅱ来除硫,将一定量的烟气压缩到一个20L的容器中,测得不同温度下,容器内SO2的质量(mg)如下表:
| 时间/min SO3/mg 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| T1 | 2100 | 1052 | 540 | 199 | 8.7 | 0.06 | 0.06 |
| T2 | 2100 | 869 | 242 | x | x | x | x |
②若其它条件都相同T1< T2,《填“>”、“<”或“=”下同);x>0.06.
③在T2温度下,若平衡后将容器的容器压缩为10L,则新平衡时SO2的浓度平衡时SO2的浓度=(填“>”、“C”或“=”)理由是该反应的平衡常数表达式为K=$\frac{1}{c(S{O}_{2})}$,温度不变,K不变,所以浓度相等.

 铁氰化钾{K3[Fe(CN)6]}俗称赤血盐,常用于检验Fe3+,遇Fe2+生成深蓝色沉淀,离子反应方程式为:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓.回答下列问题:
铁氰化钾{K3[Fe(CN)6]}俗称赤血盐,常用于检验Fe3+,遇Fe2+生成深蓝色沉淀,离子反应方程式为:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓.回答下列问题:
 ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是_________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是_________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。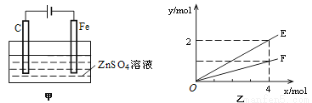
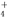 完全转化为NH3逸出,另取一份加入含bmolHCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为
完全转化为NH3逸出,另取一份加入含bmolHCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为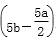 mol/L D.
mol/L D. mol/L
mol/L 2H2(g)+O2(g)ΔH1=571.6kJ/mol
2H2(g)+O2(g)ΔH1=571.6kJ/mol