题目内容
14.设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )| A. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA | |
| B. | 常温下,16gO2和O3的混合气体中含有的氧原子数为NA | |
| C. | 标准状况下,22.4 L NO 和22.4 L O2混合后所得气体中分子总数为1.5 NA | |
| D. | 1molFeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 |
分析 A.醋酸是弱酸部分电离;
B.氧气和臭氧都是氧原子构成,氧原子物质的量n=$\frac{16g}{16g/mol}$=1mol;
C.一氧化氮与氧气反应生成二氧化氮,二氧化氮与四氧化二氮之间存在转化平衡,所以反应后的物质中含有的分子数减小;
D.胶体微粒是氢氧化铁的集合体.
解答 解:A..醋酸是弱酸部分电离,0.1L0.5mol/LCH3COOH溶液中含有的氢离子数小于0.05NA,故A错误;
B.氧气和臭氧均由氧原子构成,16gO2和O3的混合气体中氧原子的物质的量为1 mol,氧原子数为NA,故B正确;
C.根据2NO+O2═2NO2可知:标准状况下,22.4 L NO即1molNO 和22.4 L O2 即1mol氧气混合后所得气体的物质的量为1.5mol,但由于NO2气体中存在平衡:2NO2?N2O4,导致分子总数小于1.5 NA,故C错误;
D.Fe(OH)3胶粒是氢氧化铁的微粒集合体,1molFeCl3与沸水反应生成胶体后,含有Fe(OH)3胶粒<NA个,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的应用,质量换算物质的量计算微粒数,气体摩尔体积的条件应用,胶体微粒的组成,熟练掌握概念和计算,即可解决,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.关于电解法精炼铜的下列说法正确的是( )
| A. | 电解过程中阴极发生氧化反应 | B. | 电解结束后,溶液中Cu2+浓度变大 | ||
| C. | 粗铜作阳极,硫酸铜为电解质溶液 | D. | 纯铜作阳极,硫酸铜为电解质溶液 |
5.Al、Fe都是重要的金属元素.下列说法正确的是( )
| A. | 两者对应的氧化物均为碱性氧化物 | |
| B. | 两者的单质都不能与氢氧化钠溶液反应 | |
| C. | 常温条件下,两种金属都能溶解于浓硫酸中 | |
| D. | 制备AlCl3、FeCl3,均不能采用将其溶液直接蒸干的方法 |
2.若烷烃CH3CH2CH(CH3)CH(CH3)CH2CH3是烯烃与氢气的加成产物,烯烃可能的结构有a种,若该烷烃是炔烃与氢气的加成产物,炔烃可能的结构有b种,则a、b分别等于( )
| A. | 7、2 | B. | 7、1 | C. | 4、2 | D. | 4、1 |
19.某有机物1.8g在氧气中完全燃烧,只生成2.64g CO2和1.08H2O,下列说法正确的是( )
| A. | 该有机物仅含有碳、氢两种元素 | |
| B. | 该有机物中碳、氢原子的个数比是1:1 | |
| C. | 该有机物中一定含有氧元素 | |
| D. | 可以确定出该有机物的分子式 |
6.${\;}_{92}^{235}$U是重要的核工业原料,下列关于${\;}_{92}^{235}$U说法正确的是( )
| A. | ${\;}_{92}^{235}$U原子核中含有92个中子 | B. | ${\;}_{92}^{235}$U原子核外有143个电子 | ||
| C. | ${\;}_{92}^{235}$U的质量数为92 | D. | ${\;}_{92}^{235}$U与${\;}_{92}^{238}$U互为同位素 |
3.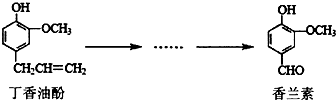 香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )
香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )
 香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )
香兰素是重要的香料之一,它可由丁香油酚经多步反应合成(见如图).有关上述两种化合物的说法不正确的是( )| A. | 在丁香油酚分子中至少有12个原子共平面 | |
| B. | 常温下,1mol丁香油酚可与2molBr2反应 | |
| C. | 1moI香兰素最多能与4mol氢气发生加成反应 | |
| D. | 可用酸性KMnO4溶液检验丁香油酚中是否含有碳碳双键 |
7.NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下,40gSiC中含有Si-C键的数目为NA | |
| B. | 标准状况下,5.6LO2含有4 NA个电子 | |
| C. | 53.5gNH4Cl中含有H-Cl键的数目为4NA | |
| D. | 25℃时,pH=13的1L Ba(OH)2溶液中含有OH-的数目为0.2NA |
 有A、B、C、D四种有机物,A、B、C都属于烃类物质,D是烃的衍生物.A是含氢量最大的有机物,分子结构为正四面体;B的球棍模型为
有A、B、C、D四种有机物,A、B、C都属于烃类物质,D是烃的衍生物.A是含氢量最大的有机物,分子结构为正四面体;B的球棍模型为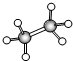 ;C的比例模型为
;C的比例模型为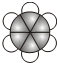 ;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应.
;D的相对分子质量为46,能与Na反应,但不能与NaOH溶液反应. CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.