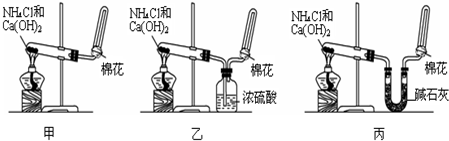
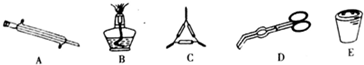
题目内容
6.设NA为阿伏加德罗常数的值,下列说法中正确的是( )| A. | 4.4 g二氧化碳含有的分子数为0.1NA | |
| B. | 锌从盐酸中置换出1 mol H2,电子转移数为NA | |
| C. | 常温常压下,11.2 L氧气含有的原子数为NA | |
| D. | 1 mol•L-1CaCl2溶液中含有的氯离子数为2NA |
分析 A、分子个数N=$\frac{m}{M}{N}_{A}$;
B、锌和盐酸反应生成氢气时,氢元素的价态由+1价变为0价;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、溶液体积不明确.
解答 解:A、分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{4.4g}{44g/mol}$×NA/mol=0.1NA个,故A正确;
B、锌和盐酸反应生成氢气时,氢元素的价态由+1价变为0价,故当生成1mol氢气时,电子转移2NA个,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氧气的物质的量小于0.5mol,则含有的原子个数小于NA个,故C错误;
D、溶液体积不明确,故溶液中的氯离子的个数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案
相关题目
14.能源可划分为一级能源和二级能源,自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取;未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列叙述正确的是( )
| A. | 水煤气,电能是一级能源 | |
| B. | 天然气,水力是二级能源 | |
| C. | 核能,煤,石油符合未来新能源标准 | |
| D. | 太阳能,生物质能,风能,氢能符合未来新能源标准 |
1.锌是人体不可缺少的微量元素之一.下列关于${\;}_{30}^{65}$Zn的说法不正确的是( )
| A. | 质子数为30 | B. | 中子数为35 | C. | 核外电子数为35 | D. | 质量数为65 |
11.下列变化过程中,没有破坏化学键的是( )
| A. | 氯化钠的融化 | B. | 乙醇溶于水 | C. | 乙烯的燃烧 | D. | 水的通电分解 |
18.下列气体中,对人体无毒害作用的是( )
| A. | Cl2 | B. | N2 | C. | NO | D. | SO2 |
15.下列物质中,能导电的是( )
| A. | 盐酸 | B. | 液态氯化氢 | C. | 干冰 | D. | 氯化钠晶体 |
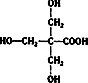 .
.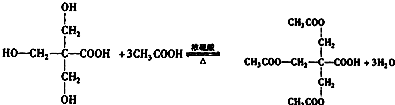 .
. .
.