��Ŀ����
10�� ��һ�̶��ݻ�Ϊ2L���ܱ������ڼ���0.2mol��N2��0.6mol��H2����һ�������·������·�Ӧ��N2��g��+3H2��g��?2NH3��g������H��0����Ӧ��NH3�����ʵ���Ũ�ȵı仯�����ͼ��ʾ����ش��������⣺
��һ�̶��ݻ�Ϊ2L���ܱ������ڼ���0.2mol��N2��0.6mol��H2����һ�������·������·�Ӧ��N2��g��+3H2��g��?2NH3��g������H��0����Ӧ��NH3�����ʵ���Ũ�ȵı仯�����ͼ��ʾ����ش��������⣺�ٸ�����ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��ƽ����Ӧ����v��NH3��=0.025mol/��L•min������ƽ��ʱת���ʦ���N2��=50%��
��������������˵��������Ӧ�Ѵ�ƽ�����BD��
A��3v����H2��=2v����NH3��
B�������������ƽ����Է���������ʱ����仯
C��������������ܶȲ���ʱ����仯
D������������ķ�����������ʱ����仯
E��N2��H2��NH3��������ͬʱ����
F��N2��H2��NH3��Ũ�ȱ�Ϊ1��3��2
G������1mol N��N��ͬʱ�γ�6mol N-H
�۱�����ͬ����������ʼʱ���������г���0.1mol��N2���ﵽ��ƽ��ʱNH3�İٷֺ�����ԭƽ����ͬ������ʼ��Ӧ����H20.3mol��NH30.2 mol��������ͬ����������ʼʱ���������г���0.8mol��NH3�����ƽ��ʱNH3�������������ԭƽ��NH3���������������ڡ�����С�ڡ����ڡ�����
�ܵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ�⣨��ʱNH3Ũ��ԼΪ0.25mol/L����������ͼ�л�����5����ĩ����ƽ��ʱNH3Ũ�ȵı仯���ߣ�
���� ����ͼ��֪��4minʱ����ƽ�⣬ƽ��ʱ������Ũ��Ϊ0.1mol/L������v=$\frac{��c}{��t}$����v��NH3����
���ɰ���Ϊ0.1mol/L��2L=0.2mol�����ݷ���ʽ����ת���ĵ������ʵ������������㵪��ת���ʣ�
�ڿ��淴Ӧ����ƽ��ʱ��ͬ�����ʵ�����������ȣ�����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����仯˵������ƽ�⣻
�ۺ��º����£�����ʼʱ���������г���0.1mol��N2���ﵽ��ƽ��ʱNH3�İٷֺ�����ԭƽ����ͬ����ԭƽ��Ϊ��Чƽ�⣬����ѧ��������ȫת������ߣ�����N2Ϊ0.2mol��H2Ϊ0.6mol��
������ͬ����������ʼʱ���������г���0.8mol��NH3����Ч��ʼͨ��0.4mol��N2��1.2mol��H2����ЧΪ��ԭƽ��Ļ���������ѹǿ����ԭƽ����ȣ�ƽ�������ƶ���
�ܵ�5����ĩ�������������Сһ�룬˲�䰱����Ũ�ȱ�Ϊԭ����2����ѹǿ����ƽ��������Ӧ�ƶ���8minĩ�ﵽ�µ�ƽ�⣬��ʱNH3Ũ��ԼΪ0.25mol/L���ݴ���ͼ��
��� �⣺����ͼ��֪��4min��ƽ�⣬��c��NH3��=0.1mol/L������v��NH3��=$\frac{0.1mol/L}{4min}$=0.025mol/��L•min����
���ɰ���Ϊ0.1mol/L��2L=0.2mol�����ݷ���ʽ��֪ת���ĵ������ʵ���Ϊ0.2mol��$\frac{1}{2}$=0.1mol������ת����Ϊ$\frac{0.1mol}{0.2mol}$��100%=50%��
�ʴ�Ϊ��0.025mol/��L•min����50%��
��A����ͬ���ʱ�ʾ������֮�ȵ��뻯ѧ������֮�ȣ���Ӧ����ƽ��״̬��3v����H2��=2v����NH3����v����H2����v����NH3��=2��3�������ڻ�ѧ������֮�ȣ�δ����ƽ��״̬���淴Ӧ���ʽϴ�ƽ�����淴Ӧ���У���A����
B����Ӧ�����������������䣬�淴Ӧ���У��ܵ����ʵ�����С����ƽ����Է���������С�������������ƽ����Է���������ʱ����仯��˵������ƽ��״̬����B��ȷ��
C����Ӧ�����������������䣬�������ݻ����䣬�ܶ�ʼ�ղ��䣬������������ܶȲ���ʱ����仯����˵������ƽ��״̬����C����
D������Ӧ���������ʵ�����С�ķ�Ӧ���淴Ӧ�������������Ŀ���٣�����������ķ�����������ʱ����仯��˵������ƽ��״̬����D��ȷ��
E����Ӧ���к�δ�ﵽƽ��N2��H2��NH3��������Ҳͬʱ���ڣ���E����
F��N2��H2��NH3��Ũ�ȱ�����ʼŨ�ȼ�ת�����йأ�ƽ��ʱ��һ�����ڻ�ѧ������֮�ȣ���F����
G������1mol N��N��ͬʱ�γ�6mol N-H������ʾ����Ӧ���ʣ���Ӧʼ�հ��ñ�����ϵ���У�ƽ��ʱ����1mol N��N��ͬʱ����6mol N-H����G����
��ѡ��BD��
�ۺ��º����£�����ʼʱ���������г���0.1mol��N2���ﵽ��ƽ��ʱNH3�İٷֺ�����ԭƽ����ͬ����ԭƽ��Ϊ��Чƽ�⣬����ѧ��������ȫת������ߣ�����N2Ϊ0.2mol��H2Ϊ0.6mol����
0.1mol+$\frac{1}{2}$��n��NH3��=0.1mol��n��H2��+$\frac{3}{2}$n��NH3��=0.6mol
���n��NH3��=0.2mol��n��H2��=0.3mol
������ͬ����������ʼʱ���������г���0.8mol��NH3����Ч��ʼͨ��0.4mol��N2��1.2mol��H2����ЧΪ��ԭƽ��Ļ���������ѹǿ����ԭƽ����ȣ�ƽ�������ƶ������ƽ��ʱNH3�������������ԭƽ��NH3�����������
�ʴ�Ϊ��0.3��0.2�����ڣ�
�ܵ�5����ĩ�������������Сһ�룬˲�䰱����Ũ�ȱ�Ϊԭ����2����ѹǿ����ƽ��������Ӧ�ƶ���8minĩ�ﵽ�µ�ƽ�⣬��ʱNH3Ũ��ԼΪ0.25mol/L����5����ĩ������ƽ��ʱNH3Ũ�ȵı仯����Ϊ��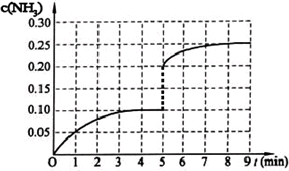 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼�黯ѧ��Ӧ���ʵļ��㡢��ѧƽ��̬���жϡ���Чƽ�⡢Ӱ�컯ѧƽ������صȣ��Ѷ��еȣ�ע���ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯������˵������ƽ�⣮

| A�� | һ�����ڵ�������Na+��SO32-��NO3-��AlO2- | |
| B�� | һ�����ڵ�������Na+��SO32-��CO32-��AlO2- | |
| C�� | ���ܴ��ڵ�������Al3+��CO32- | |
| D�� | ���ܴ��ڵ�������CO32-��S2- |
| A�� | CH4��g��+2O2��g���TCO2��g��+H2O��l����H=-890kJ | |
| B�� | ��ʾH2S����ȼ���ȵ��Ȼ�ѧ����ʽΪ��2H2S��g��+O2��g���T2S��s��+2H2O��l����H=-136kJ/mol | |
| C�� | 2mol H2ȼ�յ�ˮ��������484 kJ����H2O��g���TH2��g��+1/2O2��g����H=+242 kJ/mol | |
| D�� | 2NO+O2=2NO2 ��H=+116.2kJ/mol |
| A�� | SO2Ϊ0.4mol/L��O2Ϊ0.2mol/L | B�� | SO2Ϊ0.25mol/L | ||
| C�� | SO2��SO3��Ϊ0.15molL | D�� | SO3Ϊ0.4mol/L |
| A�� | ��ȥMgCl2��Һ��������FeCl3����ѡ��MgO | |
| B�� | Na�������������������NaHCO3 | |
| C�� | ��������ͭ�ڿ����г�ʱ����ã������ֻ���������� | |
| D�� | ��NaOH��Һ����μ�����������FeCl3��Һ�����Ƶ�Fe��OH��3���� |
| ��� | ��Ӧ�� | ���� |
| �� | Cl2��H2O2 | Cl- |
| �� | Cl2��FeI2 | FeCl2��I2 |
| �� | KClO3��HCl | Cl2��KCl��H2O |
| A�� | �ڢ��鷴Ӧ����������ΪO2 | |
| B�� | �ڢ��鷴Ӧ��Cl2 ��FeI2�����ʵ���֮��С�ڻ����1��1 | |
| C�� | �ڢ��鷴Ӧ������1molCl2ת��6mol���� | |
| D�� | ��������ǿ������˳��ΪClO3-��Cl2��I2 |
| A�� | �ڶƼ��϶�п����п������ | |
| B�� | ��ⱥ��ʳ��ˮ��̼�������� | |
| C�� | ������ڵ��Ȼ�����ȡ������������������ | |
| D�� | ��ⷨ����ͭ���ô�ͭ������ |
 ��������͵����������dz��õĻ���ԭ�ϣ���Ҳ�Ǵ�������Ҫ��Ⱦ��ۺ���������Ⱦ�ǻ�����ѧ��ǰ����Ҫ�о�����֮һ��
��������͵����������dz��õĻ���ԭ�ϣ���Ҳ�Ǵ�������Ҫ��Ⱦ��ۺ���������Ⱦ�ǻ�����ѧ��ǰ����Ҫ�о�����֮һ��