题目内容
9.A~G是几种烃分子的球棍模型(如图),据此回答下列问题:
(1)常温下含氢量最高的烃是(填对应字母)A;
(2)能够发生加成反应的烃有(填数字)4种;
(3)G与浓硝酸和浓硫酸的混酸共热生成的淡黄色晶体的名称(用系统命名法命名)2,4,6-三硝基甲苯;(不允许写简称)
(4)写出A失去一个氢原子形成的甲基的电子式
 ;
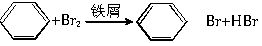
;(5)写出F发生溴代反应的化学方程式:
 .
.(6)写出实验室制取D的化学方程式CaC2+2H2O→Ca(OH)2+C2H2↑.
分析 由结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,根据物质的组成、结构和性质解答该题.
解答 解::有结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,
(1)常温下含氢量最高的气态烃是为甲烷,故答案为:A;
(2)能够发生加成的烃有有乙烯、乙炔、苯和甲苯4种,故答案为:4;
(3)G与浓硝酸和浓硫酸的混酸共热生成的淡黄色晶体,为2,4,6-三硝基甲苯,故答案为:2,4,6-三硝基甲苯;
(4)A失去一个电子为甲基,电子式为 ,故答案为:
,故答案为: ;
;
(5)F为苯,可与溴发生取代反应,反应的方程式为 ,
,
故答案为: ;
;
(6)D为乙炔,实验室用碳化钙和饱和食盐水制备,反应的方程式为CaC2+2H2O→Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握有机物的结构特点,根据结构模型判断有机物的种类,为解答该题的关键.

练习册系列答案
相关题目
19.海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:下列说法不正确的是( )
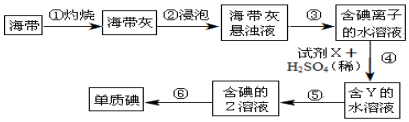

| A. | ③步操作中所用到的玻璃仪器有:漏斗、烧杯、玻璃棒 | |
| B. | ④步反应的离子方程式可以是:2I-+H2O2+2H+=I2+2H2O | |
| C. | ⑤步的操作名称是萃取与分液,其中Z是萃取剂,Z可以是乙醇 | |
| D. | ⑥步的操作名称是蒸馏 |
20.下列分离或提纯物质的方法正确的是( )
| A. | 用溶解、过滤的方法提纯含有少量 BaSO4 的 BaCO3 | |
| B. | 用过滤的方法除去 NaCl 溶液中含有的少量淀粉胶体 | |
| C. | 用渗析的方法精制 Fe(OH)3 胶体 | |
| D. | 用分液的方法分离水和酒精 |
4.下列叙述正确的是( )
| A. | 强电解质都是离子化合物,弱电解质都是共价化合物 | |
| B. | 强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子 | |
| C. | 向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体 | |
| D. | 向Na2CO3饱和溶液中,通入过量的CO2后,加热蒸干得NaHCO3晶体 |
1.设NA为阿伏加德罗常数的值,下列说法一定正确的是( )
| A. | 0.1mol FeCl3能形成的胶体粒子数为0.1NA | |
| B. | 常温下1L pH=12氨水中含有OH-数目为0.01NA | |
| C. | 0.1mol02完全反应时,转移的电子数为0.4NA | |
| D. | 12克碳单质中所含的共价键数为2NA |
18.下列有关离子方程式正确的是( )
| A. | 将氟气通入水中:F2+H2O═H++F++HFO | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═2Fe3++Fe2++4H2O | |
| C. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| D. | 往KAl(SO4)2溶液中滴入Ba(OH)2溶液至沉淀的物质的量最大Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |