题目内容
17.宇宙飞船上使用的氢氧燃料电池是一种新型化学电池,其结构如图1所示,A、B是多孔性碳制成的两个电极.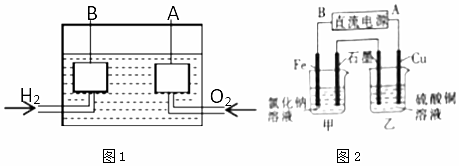
(1)该燃料电池的正极是A(填“A”或“B”),若电解质溶液为KOH溶液,则负极的电极反应式为H2+2OH--2e-=2H2O;一段时间后,溶液的pH会变小(填“变大”“变小”或“不变”).
(2)若电解质溶液为硫酸,则正极的反应式为O2+4H++4e-=2H2O.
(3)若用该氢氧燃料电池作电源电解氯化钠溶液和硫酸铜溶液,装置如图2所示,则铁电极上产生的气体为H2(填化学式);一段时间后,铜电极的质量减少6.4g,则甲池中石墨电极上产生气体的物质的量为0.1mol.
分析 (1)氢氧燃料电池中,通入氢气的一极a为电源的负极,发生氧化反应,通入氧气的一极b为原电池的正极;
(2)酸性条件下,氧气在正极上得电子生成水;
(3)Fe与负极相连作阴极,阴极上氢离子得电子;Cu与正极相连作阳极失电子生成铜离子,结合电子守恒计算.
解答 解:(1)氢氧燃料电池中,通入氢气的一极为电源的负极,通入氧气的一极为原电池的正极,由于电解质溶液呈碱性,则负极电极反应式为:2H2-4e-+4OH-=4H2O,正极电极反应式为:O2+4e-+2H2O=4OH-,电池的总反应为2H2+O2=2H2O,溶液的体积增大,溶液碱性减弱,则pH减小;
故答案为:A;2H2-4e-+4OH-=4H2O;变小;
(2)酸性条件下,氧气在正极上得电子生成水,则正极的电极方程式为:O2+4H++4e-=2H2O;
故答案为:O2+4H++4e-=2H2O;
(3)Fe与负极相连作阴极,阴极上氢离子得电子,所以阴极上生成氢气;Cu与正极相连作阳极失电子生成铜离子,电极反应为Cu-2e-=Cu2+,铜电极的质量减少6.4g,即Cu参加反应的物质的量为0.1mol,则转移电子为0.2mol,甲池中石墨电极上氯离子得电子生成氯气,由电子守恒可知,生成的氯气为0.1mol;
故答案为:H2;0.1mol.
点评 本题考查了原电池和电解池的工作原理的应用,注意把握电极名称、电极判断、电极反应、电池反应,题目难度中等,明确电子守恒在计算中的应用是解题关键.

练习册系列答案
相关题目
8.“绿色化学”的主要内容之一是使原子充分利用,不产生污染物.下列化学反应符合“绿色化学”理念的是
( )
( )
| A. | 制CuSO4:Cu+2H2SO4(浓)$\frac{\underline{\;△\;}}{\;}$CuSO4+SO2↑+2H2O | |
| B. | 制CuSO4:2Cu+O2$\frac{\underline{\;△\;}}{\;}$2CuO;CuO+H2SO4(稀)═CuSO4+H2O | |
| C. | 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | |
| D. | 制Cu(NO3)2:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O |
5.下列解释事实的方程式正确的是( )
| A. | 在空气中切开金属钠,光亮表面变暗:2Na+O2═Na2O2 | |
| B. | 向氯化铝溶液中加入过量氨水,产生白色沉淀:Al3++3OH-═Al(OH)3 | |
| C. | 将铁粉与水蒸气共热,产生气体:2Fe+3H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2O3+3H2↑ | |
| D. | Al2O3 粉末溶于 NaOH 溶液中:Al2O3+2OH-═2AlO2-+H2O |
2.下列关于结构式的叙述中正确的是( )
| A. | 表示组成分子中的各原子在空间的位置 | |
| B. | 以共价键相连的两原子间总以一条短线相连 | |
| C. | 结构式和球棍模型在表示分子结构上作用相同 | |
| D. | 用一条短线表示一对共用电子对的图式反映共价分子中各原子的连接顺序 |
6.短周期元素Q、W、X、Y、Z在元素周期表中的位置如表格所示,Z元素的简单离子半径在本周期中最小,下列说法不正确的是( )
| X | Y | |||
| Z | W | Q |
| A. | 离子半径的大小顺序为r(Q-)>r(W2-)>r(Z3+)>r(Y2-) | |
| B. | X、Q的氢化物化合的产物中既含共价键又含离子键 | |
| C. | Y氢化物的沸点比W氢化物的沸点高 | |
| D. | X、Z、W、Q的最高价氧化物对应的水化物均能与强碱反应 |
7.在含有H+、Cl-、Na+的溶液中,还可以大量共存的离子是( )
| A. | CO32- | B. | AlO2- | C. | Ca2+ | D. | Ag+ |
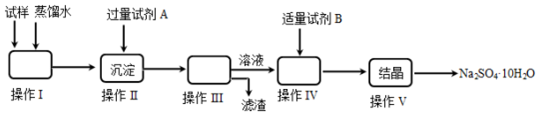

 ;
;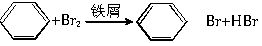 .
.