题目内容
化学反应2A+B?2C达到平衡后升高温度C的量增加,关于此反应说法正确的是( )
| A、放热反应 |
| B、吸热反应 |
| C、没有显著热量变化 |
| D、原平衡没有移动 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:根据外界条件对平衡的影响分析:升高温度向吸热方向移动.
解答:
解:升高温度,化学平衡向着吸热方向进行,即向着生成C的方向进行,故反应是吸热反应,
故选B.
故选B.
点评:本题考查了外界条件对平衡的影响,考查学生对基础知识的掌握情况,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
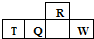 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A、最简单气态氢化物的热稳定性:R>Q |
| B、最高价氧化物对应水化物的酸性:Q<W |
| C、原子半径:T>Q>R |
| D、含T的盐溶液加入过量的氨水一定可以产生沉淀 |
L-T5种短周期元素的信息如表,有关叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、+4、-2 | -2 |
| A、与稀盐酸反应的剧烈程度:L单质<Q单质 |
| B、热稳定性:H2T<H2R |
| C、M与T形成的化合物具有两性 |
| D、L2+与R2-的核外电子数相等 |
已知金属钠投入水中发生剧烈反应,并有氢气生成.装运金属钠的包装箱应贴的图标是( )
A、 腐蚀品 |
B、 爆炸品 |
C、 遇湿易燃品 |
D、 氧化剂 |
对于xA(g)+yB(g)?zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法中正确的是( )
①x+y>z+w,正反应是放热反应 ②x+y>z+w,正反应是吸热反应
③x+y<z+w,逆反应是放热反应 ④x+y<z+w,逆反应是吸热反应.
①x+y>z+w,正反应是放热反应 ②x+y>z+w,正反应是吸热反应
③x+y<z+w,逆反应是放热反应 ④x+y<z+w,逆反应是吸热反应.
| A、①② | B、③④ | C、①③ | D、②④ |
下列叙述中正确的是( )
| A、含最高价元素的化合物,一定具有强氧化性 |
| B、阳离子只有氧化性,阴离子只有还原性 |
| C、失电子越多,还原性越强 |
| D、属于氧化还原反应的化合反应不一定是因为有单质参与了反应 |
有关胶体和溶液的比较中正确的是( )
| A、溶液呈电中性,胶体带有电荷 |
| B、Fe(OH)3胶体粒子在电场影响下将向阳极运动 |
| C、溶液中通过光束没有特殊现象,胶体中通过光束有丁达尔现象 |
| D、通电后,溶液中溶质粒子一定分别向两极移动,而胶体中分散质粒子向某一极移动 |
100℃下,某反应达到平衡,平衡常数K=
.恒容时,升高温度,NO浓度减小.下列说法正确的是( )
| c(NO)?c(SO3) |
| c(NO2)?c(SO2) |
| A、该反应的焓变为正值 |
| B、恒温下减小压强,反应体系的颜色加深 |
| C、升高温度,逆反应速率减小 |
| D、该反应化学方程式为NO2+SO?NO+SO3 |
将Al片和Cu片用导线相连,一组插入浓盐酸中,一组插入稀氢氧化钠溶液中,分别形成原电池,则在这两原电池中,正极分别为( )
| A、Cu片、Cu片 |
| B、Cu片、Al片 |
| C、Al片、Al片 |
| D、Al片、Cu片 |