题目内容
19.乙烯是重要化工原料,其产量是一个国家石油化工水平的标志.通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品.已知乙烯能发生以下转化: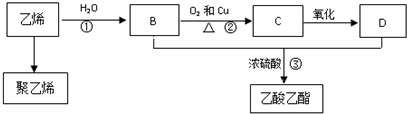
(1)乙酸乙酯的分子式为C4H8O2;乙烯的结构简式为CH2=CH2.
(2)反应①的反应类型是加成反应,D物质的官能团名称为羧基.
(3)写出以下反应的化学方程式:
①CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
②2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
③C2H5OH+CH3COOH
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.
分析 乙烯和水发生加成反应生成B,B为CH3CH2OH,B被催化氧化生成C,C为CH3CHO,C被氧化生成D,D为CH3COOH,B、D发生酯化反应生成乙酸乙酯,乙烯发生加聚反应生成聚乙烯,以此解答该题.
解答 解:乙烯和水发生加成反应生成B,B为CH3CH2OH,B被催化氧化生成C,C为CH3CHO,C被氧化生成D,D为CH3COOH,B、D发生酯化反应生成乙酸乙酯,乙烯发生加聚反应生成聚乙烯,
(1)乙酸乙酯分子式为C4H8O2,乙烯结构简式为CH2=CH2,故答案为:C4H8O2;CH2=CH2;
(2)反应①为i加成反应,D为乙酸,含有羧基,故答案为:加成反应;羧基;
(3)①乙烯和水加成反应生成乙醇,反应的方程式为CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
②反应为乙醇的催化氧化,反应方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
③是乙醇和乙酸的酯化反应生成乙酸乙酯,反应方程式为C2H5OH+CH3COOH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;C2H5OH+CH3COOH CH3COOC2H5+H2O.
CH3COOC2H5+H2O.
点评 本题考查有机物推断,为高频考点,侧重于学生的分析能力的考查,本题涉及烯、醇、醛、羧酸之间的转化关系等,难度不大,注意基础知识的理解掌握.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
10.常温下,下列各组离子或分子组能大量共存且满足相应要求的是( )
| 选项 | 离 子 | 要 求 |
| A | K+、AlO2-、Cl-、MnO4- | c(K+)<c(Cl-) |
| B | Fe3+、NO3-、I-、HCO3- | 逐滴加入盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、CH2COOH | 逐滴加入NaOH溶液立即有气体产生 |
| D | Na+、Cu2、Cl-、SO42- | 逐滴加氨水先有沉淀产生,后沉淀消失 |
| A. | A | B. | B | C. | C | D. | D |
11.我国科学家屠呦呦因在青蒿素发现和治疗中的贡献,获得了诺贝尔生理学或医学奖,青蒿素是一种治疗疟疾的特效药.由植物黄花蒿叶中提取的青蒿素还可合成用于抗氯喹恶性疟及凶险型疟疾的蒿甲醚,其合成路线如下:
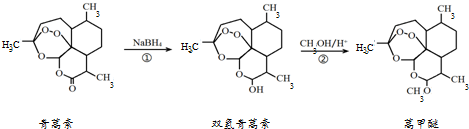
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 青蒿素的分子式是C15H21O5 | |
| B. | 青蒿素在NaOH溶液中可以发生水解反应 | |
| C. | 反应②有H2O生成 | |
| D. | 青蒿素分子内的“-O-O-”基团可能对疟原虫有抑制作用 |
8.下列电解质溶液中,微粒的物质的量浓度关系一定正确的是( )
| A. | 在0.1 mol•L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 在0.1 mol•L-1NaClO溶液中:c(OH-)=c(H+)+c(HClO) | |
| C. | 25℃时,0.1 mol•L-1CH3COOH溶液中滴入NaOH溶液,使溶液pH=7时:c(CH3COO-)=c(Na+)>c(H+)=c(OH-) | |
| D. | 已知酸性:HCOOH>CH3COOH,浓度均为0.1 mol•L-1的HCOOK与CH3COONa溶液中:c(K+)-c(HCOO-)>c(Na+)-c(CH3COO-) |
9.对下列物质中锰元素化合价的判断,正确的是( )
| A. | KMnO4中为+3 | B. | MnSO4中为-2 | C. | K2MnO4中为+6 | D. | MnO2中为+2 |
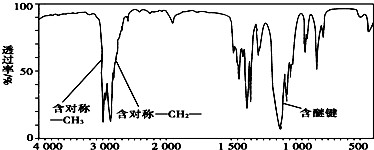
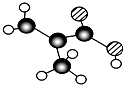 ,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).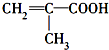 .
.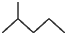 表示的有机物C的分子式为C6H14.
表示的有机物C的分子式为C6H14.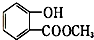 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.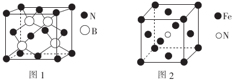
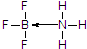 (标注出其中的配位键);利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,图1为该晶体的晶胞结构,该功能陶瓷晶体的化学式为BN.
(标注出其中的配位键);利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,图1为该晶体的晶胞结构,该功能陶瓷晶体的化学式为BN.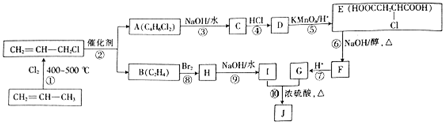
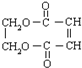 .
. +3NaOH$→_{△}^{醇}$NaOOC-CH=CH-COONa+NaCl+3H2O.
+3NaOH$→_{△}^{醇}$NaOOC-CH=CH-COONa+NaCl+3H2O.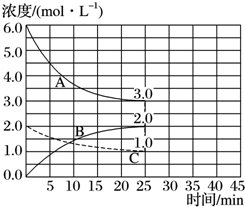 (1)目前工业合成氨的原理是N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ•mol-1.
(1)目前工业合成氨的原理是N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ•mol-1.