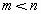题目内容
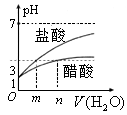
体积相同、浓度均为0.2mol/L的盐酸和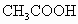 溶液,分别加水稀释10倍,溶液的pH分别变为m和n,则m与n的大小关系为________。
溶液,分别加水稀释10倍,溶液的pH分别变为m和n,则m与n的大小关系为________。
答案:略
解析:
提示:
解析:
|
 。 。
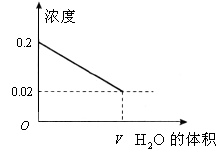
一变:体积相同、浓度均为0.2mol/L的盐酸和醋酸溶液,分别加水稀释m倍和n倍,溶液的pH都变为3,则m与n的大小关系为________。 解:m>n 由图可知,若两者稀释相同的倍数,盐酸的pH小于醋酸的pH;若要两者的pH相等,则盐酸稀释的倍数大于醋酸稀释的倍数,故有m>n。 二变:体积相同、pH均为1的盐酸和 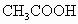 溶液,分别加水稀释m倍和n倍,溶液pH都变为3,则m与n的大小关系为________。 溶液,分别加水稀释m倍和n倍,溶液pH都变为3,则m与n的大小关系为________。
解: 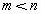 pH为1的盐酸溶液完全电离,当其稀释100倍时pH为3。醋酸为弱酸,pH为1时稀释100倍后的pH小于盐酸溶液稀释后的pH。因为 pH为1的盐酸溶液完全电离,当其稀释100倍时pH为3。醋酸为弱酸,pH为1时稀释100倍后的pH小于盐酸溶液稀释后的pH。因为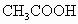 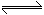 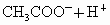 ,又电离出 ,又电离出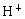 ,所以应继续加水稀释使pH增大至和盐酸的相等。本题用图像分析更为清晰,图为pH=1的盐酸和醋酸稀释过程的图像。若稀释后溶液的pH都变成3(画一条平行于横轴的水平线),易得 ,所以应继续加水稀释使pH增大至和盐酸的相等。本题用图像分析更为清晰,图为pH=1的盐酸和醋酸稀释过程的图像。若稀释后溶液的pH都变成3(画一条平行于横轴的水平线),易得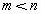 。 。
规律总结: 外界条件对弱电解质电离平衡移动的影响是高考考查的重点和热点问题,很多同学搞不清移动的结果。本题用图像法求解克服了问题分析上的障碍,也很容易理解和掌握。同时通过对一题多变的训练,巩固对易混基础知识的理解,培养同学们的审题能力和发散性思维。 |
提示:
|
题眼点拨:本题中原题及变式题均可利用强、弱电解质的不同特点来分析。 |

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目