题目内容
5.某学生欲用12mol•L-1浓盐酸和蒸馏水配制500mL物质的量浓度为0.3mol•L-1的稀盐酸.①该学生需要量取12.5mL上述浓盐酸进行配制.
②配制过程中正确的操作顺序是(字母表示,每个字母只能用一次)BCAFED;
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
③下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填“偏大”、“偏小”、“无影响”).
a.用量筒量取浓盐酸时俯视观察凹液面偏小
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水偏小
c.稀释浓盐酸时,未冷却到室温即转移到容量瓶中偏大
d.将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中偏大
e.容量瓶洗涤干净后未干燥无影响
④若在标准状况下,将V LHCl气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρ g/mL,则此溶液中HCl物质的量浓度为$\frac{1000ρV}{36.5V+22400}$mol/L.
分析 ①根据稀释前后溶液中溶质的物质的量不变来计算;
②依据配制一定物质的量浓度溶液的一般操作步骤排序;
③分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行分析,凡是使n偏大或者使V偏小的操作都会使溶液浓度偏高,反之使溶液浓度偏低;
④分别计算V LHCl的物质的量,和溶液的体积,注意溶液体积依据V=$\frac{m}{ρ}$计算,依据C=$\frac{n}{V}$计算溶液物质的量浓度.
解答 解:①设需要浓盐酸体积为V,则稀释前后溶液中溶质的物质的量不变,可知:V×12mol/L=0.3mol/L×500mL,解得V=12.5;
故答案为:12.5;
②配制一定物质的量浓度溶液的一般操作步骤:计算、量取、稀释、移液、洗涤、移液、定容、摇匀、贴签,所以正确的顺序为:BCAFED;
故答案为:BCAFED;
③a.用量筒量取浓盐酸时俯视观察凹液面,导致量取的浓盐酸体积偏小,溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏小;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,导致溶液体积偏大,溶液浓度偏低;
故答案为:偏小;
c.稀释浓盐酸时,未冷却到室温即转移到容量瓶中,冷却后液面下降,溶液体积偏小,溶液浓度偏高;
故答案为:偏大;
d.将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中,导致量取的浓盐酸体积偏大,溶质的物质的量偏大,溶液的浓度偏大;
故答案为:偏大;
e.容量瓶洗涤干净后未干燥,对溶质的量和溶液体积都不产生影响,溶液浓度不变;
故答案为:无影响;
④在标准状况下,将V LHCl物质的量n=$\frac{V}{22.4}$mol;
标准状况下,将V LHCl气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρ g/mL,则溶液的质量m=($\frac{V}{22.4}$×36.5+1000);
溶液的体积V=$\frac{\frac{V}{22.4}×36.5+1000}{1000ρ}$;
则溶液的物质的量浓度C=$\frac{n}{V}$=$\frac{1000ρV}{36.5V+22400}$mol/L;
故答案为:$\frac{1000ρV}{36.5V+22400}$.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和实验操作步骤是解题关键,注意有关气体溶于水时所得溶液的体积计算方法,题目难度不大.

| A. | 反应中H2O2被氧化 | |
| B. | CNO-中N的化合价为-3价 | |
| C. | 温度越高越有利于该反应发生 | |
| D. | 每生成1.8 g H2O,转移电子数为0.4NA |
| A. | 蒸馏操作时,冷凝水的方向应当由下往上 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 蒸馏时,应使温度计水银球位于蒸馏烧瓶的支管口处 | |
| D. | 分液操作时,首先要打开分液漏斗的上口瓶塞,或使瓶塞上的凹槽与上口部的小孔对准,然后进行分液 |

| A. | 只有① | B. | 只有①④ | C. | 只有①⑤ | D. | ①②③④⑤ |
①氯气 ②液氯 ③新制氯水 ④敞口放置的久置氯水 ⑤盐酸⑥用盐酸酸化的漂白粉溶液.
| A. | ①②③ | B. | ①②③⑥ | C. | ③⑥ | D. | ③④⑥ |
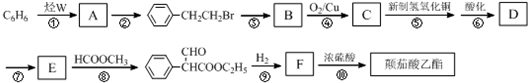
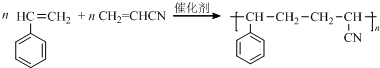 .
. .
.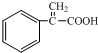 .
.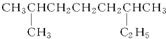 系统命名:2,6二甲基辛烷;
系统命名:2,6二甲基辛烷; ;
; ;②乙醛与银氨溶液水浴加热CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O;
;②乙醛与银氨溶液水浴加热CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O;