题目内容
8.写出下列物质的摩尔质量:Na2CO3106 g/mol CuSO4•5H2O250 g/mol CO244 g/mol.
分析 摩尔质量以g/mol作单位数值上等于其相对分子质量,相对分子质量为构成分子的各原子的相对原子质量之和,据此解答.
解答 解:根据Na2CO3化学式可知其相对分子质量=23×2+12+16×3=106,摩尔质量为106g/mol,
根据CuSO4•5H2O化学式可知其相对分子质量=64+32++16×4+5×(1×2+16)=250,其摩尔质量为250g/mol,
根据CO2化学式可知其相对分子质量=12+16×2=44,摩尔质量为44g/mol,
故答案为:106 g/mol;250 g/mol;44 g/mol.
点评 本题考查了摩尔质量的计算,明确摩尔质量与相对分子质量的关系是解本题关键,题目难度不大.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
14.电泳时,硫化砷胶粒移向正极.要使一定量硫化砷溶液聚沉下列盐中需用的物质的量最小的是( )
| A. | NaCl | B. | CaCl2 | C. | AlCl3 | D. | MgSO4 |
13.王老师在某次实验中制得下列四种不同质量的气体.则在他制得的四种气体中分子数目最多的是( )
| A. | 1gH2 | B. | 11gCO2 | C. | 8gO2 | D. | 4.5gH2O(g) |
17.在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3-、Fe2+、NH4+、H+和H2O,下列叙述正确的是( )
| A. | 为防止Fe2+水解,Fe(NO3)2溶液需要加酸酸化 | |
| B. | 该反应中氧化剂与还原剂物质的量之比为8:1 | |
| C. | 若有1molNO3-发生氧化反应,则转移电子5mol | |
| D. | 该反应中Fe2+是还原剂,NH4+是还原产物 |
18.25°C时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | c(H+)=1×10-13mol/L的溶液中:K+、Na+、NO3-、CH3COO- | |
| C. | 0.1mol•L-1NH4HCO3溶液:Na+、Fe3+、NO3-、Cl- | |
| D. | 0.1mol•L-1FeCl3溶液:Fe2+、NH4+、SCN-、SO42- |
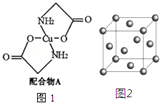 已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A.其结构如图1所示
已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A.其结构如图1所示 .
.