题目内容
6.香烟燃烧产生的烟气中含有尼古丁(化学式C10H14N2)、焦油、一氧化碳等,下列说法中错误的是 ( 相对原子质量:C 12、H 1、N 14)( )| A. | 尼古丁中C、H、N三种元素的质量比为5:7:1 | |
| B. | 吸烟有害健康 | |
| C. | CO比O2更易同血红蛋白结合,会导致人体缺氧 | |
| D. | 尼古丁中氮元素的质量分数约为17.3% |
分析 A.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
B.根据香烟燃烧产生的烟气中含有许多强致癌物质和有害物质,进行判断;
C.一氧化碳极易与血液里的血红蛋白结合,使人体缺氧;
D.根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:A.化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得尼古丁中碳、氢、氮三种元素质量比为60:7:14,故A错误;
B.香烟燃烧产生的烟气中含有许多强致癌物质和有害物质,故B正确;
C.一氧化碳极易与血液里的血红蛋白结合,使人体缺氧、窒息,甚至死亡;故C正确;
D、尼古丁中氮元素的质量分数为:$\frac{14×2}{162}$×100%≈17.3%,故D正确;
故选A.
点评 本题考查元素质量分数的计算、吸烟对人体的危害、一氧化碳的毒性等知识,题目难度不大,注意了解吸烟对人体的危害,明确元素质量分数的计算方法.

练习册系列答案
相关题目
17.下列说法不正确的是( )
| A. | 能够发生有效碰撞的分子叫做活化分子,活化分子所多出的那部分能量称作活化能 | |
| B. | 对于某一反应aA+bB=cC+dD,△H单位中的mol-1是指每摩尔(aA+bB=cC+dD)反应 | |
| C. | 研究有机物的组成、结构、性质、制备方法与应用的科学叫有机化学 | |
| D. | 甲烷分子具有正四面体结构的原因是碳原子的2S轨道与2P轨道发生SP杂化 |
14.向0.1mol•L-1的H2SO4溶液中滴入0.1mol•L-1过量的Ba(OH)2溶液,溶液的导电能力发生变化,其电流强度(I)随加入Ba(OH)2溶液的体积(V)的变化曲线正确的是( )
| A. |  | B. |  | C. |  | D. |  |
1.下图为矿泉水瓶上的部分说明文字,列出了饮用天然水理化指标,这里的钙、钾、钠是指( )

| A. | 原子 | B. | 分子 | C. | 单质 | D. | 元素 |
11.下列离子方程式中,不正确的是( )
| A. | 向FeCl2溶液中通入Cl22Fe2++Cl2═2Fe3++2Clˉ | |
| B. | FeCl3溶液跟过量氨水 Fe3++3NH3•H2O═Fe(OH)3↓+3NH4+ | |
| C. | 碳酸氢钙溶液跟稀硝酸 Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| D. | 钠与水的反应 2Na+2H2O═2Na++2OH-+H2↑ |
18.能用组成元素的单质直接反应得到的物质是( )
| A. | NO 2 | B. | FeCl2 | C. | SO3 | D. | FeCl3 |
15.下列反应的离子方程式中,书写正确的是( )
| A. | 钠跟水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 铁粉跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液跟稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙跟盐酸反应:CO32-+2H+═H2O+CO2↑ |
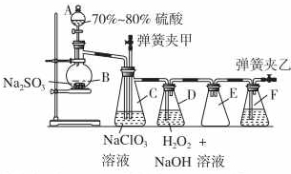 装置C中发生反应:2NaClO3+SO2═2ClO2+Na2SO4 (Ⅰ)
装置C中发生反应:2NaClO3+SO2═2ClO2+Na2SO4 (Ⅰ)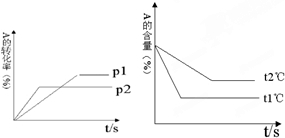 回答下列问题
回答下列问题